Ученые освоили «интуитивный» синтез антибиотиков
Американские ученые разработали метод поиска и синтезирования антибиотиков, который не требует культивирования бактерий и искусственной экспрессии генов. Результаты исследования опубликованы в журнале Nature Chemical Biology.
Антибиотики — природные или полусинтетические вещества, подавляющие рост живых клеток. Часто их действие основано на нерибосомальных пептидах — ферментах, которые производятся самими бактериями и могут синтезировать короткие пептиды без участия матричной РНК (мРНК). Поиск новых нерибосомальных пептидов и, как следствие, создание новых антибиотиков затрудняются тем, что большинство бактерий не культивируется в лабораторных условиях. И даже при успешном культивировании многие их гены, связанные с выработкой нужных веществ, остаются неактивными.
Ученые из Рокфеллеровского университета разработали метод, который позволяет синтезировать новые нерибосомальные пептиды без культивирования бактерий. На первом этапе авторы проанализировали базы данных геномов «человеческих» бактерий и с помощью пакета antiSMASH определили кластеры генов, связанные с выработкой «полезных» ферментов. После предсказания их структуры исследователи выделили 57 кластеров генов и сократили их число до 30. Наконец методом твердофазного пептидного синтеза они получили 25 химических соединений, потенциально способных выполнять функции антибиотиков.
Полученные соединения тестировались на 23 видах патогенов человека, включая некоторые стафилококки (Staphylococcus), кишечную палочку (Escherichia coli) и коринебактерию амиколатум (Corynebacterium amycolatum) — возбудителя сепсиса. На основе чувствительности микроорганизмов к препарату авторы идентифицировали два антибиотика, получившие название хьюмимицин A и хьюмимицин B. Оба соединения оказались продуктом бактерий Rhodococcus erythropolis, которые в норме являются частью микробиоты человека. Традиционные методы не позволяли выделить этот фермент.
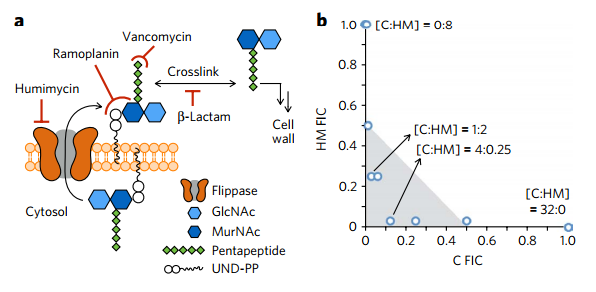
Последующий анализ показал, что хьюмимицины наиболее эффективны против стрептококков (Streptococcus) и стафилококков, в том числе метициллинрезистентного золотистого стафилококка (S. aureus). Работа пептида основана на ингибировании ферментов, необходимых микроорганизмам для синтеза клеточных стенок — в результате процесс прерывается и бактерия погибает. Аналогичный механизм используют бета-лактамные антибиотики — широкий круг препаратов, в том числе пенициллиного ряда, которые назначаются при лечении большинства инфекций. Однако к ним устойчивы некоторые патогены.
Эффективность нового антибиотика ученые проверили на культуре бактерий, а затем in vivo — на мышах, инфицированных метициллинрезистентным S. aureus. Несмотря на устойчивость к бета-лактамам, стафилококк оказался чувствителен к сочетанию бета-лактамов с хьюмимицином А (отдельно он развивал незначительные эффекты). По словам исследователей, оба соединения прерывают различные этапы одного молекулярного процесса. Соавтор работы Шон Брэди (Sean Brady) сравнил действие препаратов с «передавливанием шланга сразу в двух местах», что позволяет если не остановить, то сократить скорость протекающих процессов.
Ученые надеются, что предложенный подход поможет в разработке новых антибиотиков, в частности способных остановить самые устойчивые патогены. Метод также может применяться для изучения бактерий, которые не являются частью человеческого микробиота, а в перспективе — и бактерий, геном которых еще не отсеквенирован.
В 2017 году человечество впервые заметило объект, прилетевший из другой звездной системы. Он оказался странным, почти не похожим ни на астероид, ни на комету, и получил имя Оумуамуа. Затем появился «нормальный» межзвездный странник — комета Борисова. А в 2025-м астрономы обнаружили 3I/ATLAS — объект, который, вероятно, хранит вещество времен рождения чужих миров. Но что изменили в астрономии эти три гостя из межзвездной тьмы?
Американские биотехнологи впервые сообщили об обращении вспять клеточного старения в живых клетках печени человека — не мышиных, не синтетических, а именно человеческих. На волне этого результата компания привлекла 435 миллионов долларов и готовится к клиническим испытаниям.
Роль личности в истории чаще всего иллюстрируют правителями или полководцами. Но, глядя на современную карту мира, нельзя не признать: она выглядела бы принципиально иначе, если бы не одна крестьянская девушка, которую сожгли в этот день ровно 595 лет назад.
В 2017 году человечество впервые заметило объект, прилетевший из другой звездной системы. Он оказался странным, почти не похожим ни на астероид, ни на комету, и получил имя Оумуамуа. Затем появился «нормальный» межзвездный странник — комета Борисова. А в 2025-м астрономы обнаружили 3I/ATLAS — объект, который, вероятно, хранит вещество времен рождения чужих миров. Но что изменили в астрономии эти три гостя из межзвездной тьмы?
Астрономы провели длительную радиодиагностику межзвездного объекта 3I/ATLAS и не нашли признаков искусственных технологий. Наблюдение окончательно подтвердило естественную природу ледяного тела, хотя ученые изначально не ожидали сенсации.
Роль личности в истории чаще всего иллюстрируют правителями или полководцами. Но, глядя на современную карту мира, нельзя не признать: она выглядела бы принципиально иначе, если бы не одна крестьянская девушка, которую сожгли в этот день ровно 595 лет назад.
В высокогорных районах Гималаев появился новый хищник. Он не боится людей, возглавляет стаи собак и все чаще заходит в деревни. Местные жители называют его «кхипшанг». Речь идет о гибриде гималайского волка и бродячей собаки. Ученые опасаются, что этот зверь изменит хрупкий баланс местной дикой природы и в скором времени станет весьма опасным для человека.
В доколумбовых Андах принадлежность к правящему роду определяла доступ к земле, торговле и статусу, поэтому удержать все внутри семьи было вопросом выживания. Ученые выяснили, что элиты долины Чинча решали эту задачу самым прямым способом — заключая браки между родственниками на протяжении как минимум двух поколений.
При совпадении нескольких условий наши глаза способны улавливать излучение в ближнем инфракрасном спектре. Тогда сетчатка начинает работать как нелинейный фотодетектор.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно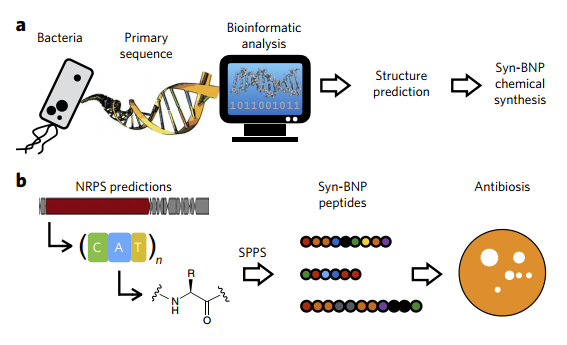







Последние комментарии