Антисмысловая терапия «болезни Хокинга» прошла доклинические тесты
Группа ученых из США объявила об успешном проведении доклинических исследований новой генной терапии бокового амиотрофического склероза (БАС) и спиноцеребеллярной атаксии.
Боковой амиотрофический склероз и спиноцеребеллярная атаксия — нейродегенеративные заболевания, которые объединяет схожая клиническая картина. В обоих случаях разрушение нейронов приводит к нарушению двигательных функций, при этом БАС также повышает риск паралича. В настоящее время универсальных способов лечения этих патологий не существует. Известно, что спиноцеребеллярная атаксия 2 типа связана с мутациями в гене ATXN2 (атаксин-2). Дефектный ген накапливает повторы триплета, который кодирует глутамин, что нарушает функции одноименного белка. На клеточном уровне это проявляется в снижении активности клеток Пуркинье, участвующих в регуляции моторики.
Новая генная терапия основана на искусственной супрессии ATXN2 в мозжечке — согласно гипотезе, это должно ослабить симптомы болезни. Чтобы проверить предположение, авторы вывели линию мышей с мутантным геном. Затем в их мозжечок вводили антисмысловые олигонуклеотиды — короткие цепочки ДНК, комплементарные атаксину. В ходе отбора различных олигонуклеотидов ученые определили наиболее оптимальный по показателю подавления. Подавление экспрессии осуществлялось за счет связывания молекул с матричной РНК (мРНК) ATXN2 и предотвращения синтеза белка. Согласно наблюдениям, ДНК, введенная в мозжечок, достигала клеток Пуркинье и уменьшала выработку дефектного атаксина. При этом нейроны животных восстановили способность к активации, а их моторика улучшилась.
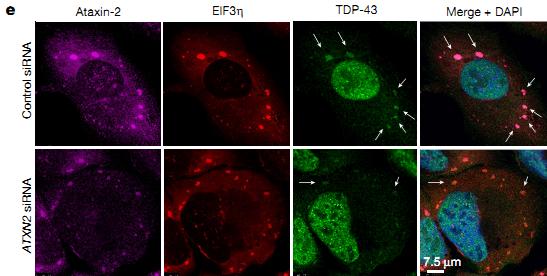
В 2012 году группа американских ученых также показала наличие связи между ATXN2 и БАС. В нейронах пациентов с боковым амиотрофическом склерозом часто наблюдается агрегация TDP-43 — ядерного белка, регулирующего транскрипцию многих генов. Исследователи обнаружили, что снижение этих белков взаимосвязано, однако механизм такой корреляции остается неясным. Предполагается, что причиной может служить способность атаксина-2 инициировать формирование стрессовых гранул, которые включают в себя РНК и связанные с ней белки, в том числе TDP-43. В новой работе авторы смоделировали у мышей БАС путем синтеза в их организме большого количества человеческого TDP-43, после чего ввели олигонуклеотид, испытанный на атаксии.
Согласно результатам, процедура повысила продолжительность жизни пострадавших особей на треть, а их двигательные функции частично восстановились. На сегодняшний день антисмысловые олигонуклеотиды одобрены властями США для лечения ряда нейродегенеративных заболеваний, например спинальной мышечной атрофии (СМА). Предположительно, после успешного завершения доклинических исследований новая терапия БАС и атаксии может вступить в первую фазу испытаний на человеке.
Подробности работ опубликованы (1, 2) в журнале Nature.
Боковой амиотрофический склероз стал широко известен благодаря истории британского физика-теоретика Стивена Хокинга. Об удивительной судьбе этого ученого читайте в нашем материале.
Исследователи опросили более 60 тысяч испытуемых из разных стран и выяснили: чем больше человек зациклен на себе, тем холоднее он к своему партнеру. Правда, снижение накала страстей не всегда плохо, у этого есть и положительные стороны.
Во время раскопок в римском лагере в Йорке (Англия) нашли стеклянную колбу, поразительно напоминающую древнеегипетские флаконы для кохля — традиционную черную подводку для глаз. Не исключено, что это средство макияжа пользовалось популярностью и у римских солдат.
В популярной литературе сверхмассивные черные дыры чаще всего представляют как разрушители звезд и планет. Авторы новой работы попробовали рассчитать, что на самом деле происходит в окрестностях таких объектов и пришли к противоположному выводу.
Вначале Reuters опубликовал статью о взаимоотношениях SpaceX и Пентагона, которую миллиардер --- традиционно для его отношений с этим изданием — назвал фейком. Опровергая ее тезисы, он обнародовал информацию, не представленную ранее публично.
Исследователи опросили более 60 тысяч испытуемых из разных стран и выяснили: чем больше человек зациклен на себе, тем холоднее он к своему партнеру. Правда, снижение накала страстей не всегда плохо, у этого есть и положительные стороны.
Провинция Цзянсу была процветающим центром медицинской практики в Китае во времена династии Мин (1368-1644 годы нашей эры). Микроскопический анализ крошечных частиц на поверхности хирургических ножниц и пинцета из гробницы китайского врача помог выявить следы вещества, получаемого из ядовитого растения, которое, по мнению исследователей, применялось как местная анестезия во время операций.
В доколумбовых Андах принадлежность к правящему роду определяла доступ к земле, торговле и статусу, поэтому удержать все внутри семьи было вопросом выживания. Ученые выяснили, что элиты долины Чинча решали эту задачу самым прямым способом — заключая браки между родственниками на протяжении как минимум двух поколений.
При совпадении нескольких условий наши глаза способны улавливать излучение в ближнем инфракрасном спектре. Тогда сетчатка начинает работать как нелинейный фотодетектор.
Вначале Reuters опубликовал статью о взаимоотношениях SpaceX и Пентагона, которую миллиардер --- традиционно для его отношений с этим изданием — назвал фейком. Опровергая ее тезисы, он обнародовал информацию, не представленную ранее публично.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно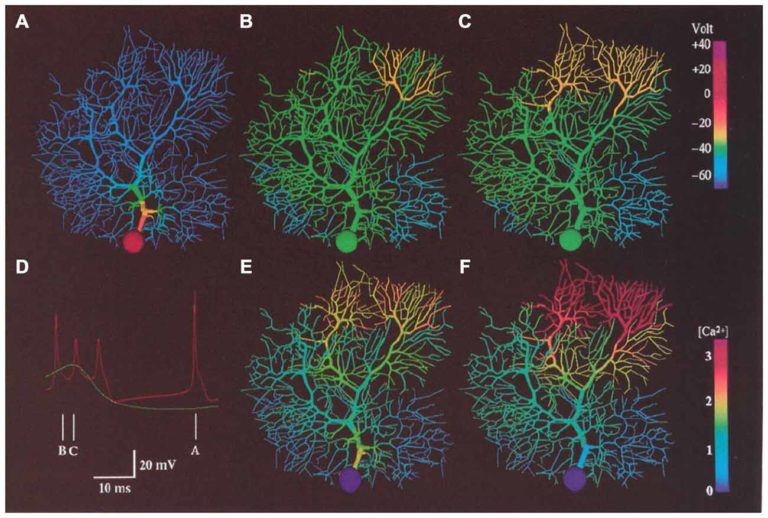








Последние комментарии