Принцип Паули: один из важнейших принципов в понимании природы вещества
Порой кажется странным, почему атомы и молекулы ведут себя определенным образом. Например, почему мы не можем проходить сквозь стены, но инфракрасное излучение через них проходит. Все может объяснить один принцип — принцип исключения Паули.
Принцип исключения Паули утверждает, что два электрона (или два любых других фермиона) не могут иметь одинаковое квантово-механическое состояние в одном атоме или одной молекуле. Другими словами, ни одна пара электронов в атоме не может иметь одинаковые электронные квантовые числа.
Этот принцип был предложен австрийским физиком Вольфгангом Паули в 1925 году для описания поведения электронов. В 1940-м он расширил принцип до всех фермионов в своей теореме о связи спина со статистикой. Бозоны — частицы с целым числом спинов — не следуют принципу исключения. Таким образом, идентичные бозоны могут занимать одно и то же квантовое состояние (как, например, фотоны в лазерах). Принцип исключения Паули применим только к частицам с полуцелым спином.
О спине проще всего думать как о вращении частицы вокруг собственной оси. Конечно, это сильное упрощение — и в реальности невозможно сказать наверняка, вращается ли на самом деле нечто столь малого размера вроде электрона. В общем говоря, спин подчиняется тем же математическим законам момента импульса, что и все вращающиеся объекты в классической физике. Здесь есть два важных момента, о которых стоит помнить: скорость вращения и направление оси, вокруг которой частица вращается (верхний или нижний спин).

Когда в 1922 году Отто Штерн и Уолтер Герлах открыли спин, их эксперименты показали, что присущий момент импульса, или спин, частицы вроде электрона квантовался, то есть мог принимать только определенные дискретные значения. Спин композитных частиц, таких как протоны, нейтроны и атомные ядра, — просто сумма спинов и орбитального момента импульса частиц, из которых они состоят, а значит, они подчиняются тем же условиям квантования. Таким образом, спин — это абсолютно квантово-механическое свойство частицы и оно не может быть объяснено классической физикой.
Позже выяснилось, что есть две подкатегории частиц: частицы с целым спином, известные сегодня как бозоны — среди которых фотоны, глюоны, W- и Z-бозоны, — а также гипотетические гравитоны и частицы с полуцелым спином: фермионы, включающие в себя электроны, нейтрино, мюоны и кварки, из которых состоят композитные частицы типа протонов и нейтронов. Различие между бозонами и фермионами можно описать тем, что у первых есть симметричные волновые функции, а у фермионов волновые функции асимметричны. Концепция частицы с полуцелым спином — очередной пример парадоксальной природы субатомных частиц: грубо говоря, фермиону нужно обернуться вокруг своей оси дважды, прежде чем он примет прежнее положение.
Важность этого различия для квантовой теории состоит в том, что волны вероятности бозонов «переворачиваются» — или инвертируются, — прежде чем успевают интерферировать друг с другом, что, по сути, и ведет к их «стадному» характеру и коллективному поведению в лазерах, сверхтекучих жидкостях и сверхпроводниках. Фермионы, однако, не переворачивают свои волны вероятности, что, помимо прочего, приводит к «асоциальному» характеру. Так и получается, что в квантовой механике складывать спины частиц нужно очень аккуратно и при помощи специальных правил вдобавок к моменту импульса.
Все вышеописанное и подводит нас к одному из важнейших принципов в квантовой механике — принципу исключения Паули. Как было сказано выше, он гласит, что два идентичных фермиона не могут занимать одно и то же квантовое состояние одновременно (хотя два электрона, например, могут приобрести противоположные спины, чтобы дифференцировать свои квантовые состояния). Этот принцип можно описать так: никакие два фермиона в квантовой системе не могут обладать одинаковыми значениями всех четырех квантовых чисел в любой момент времени. Принцип исключения Паули эффективно объясняет продолжительное существование очень высокоплотных белых карликов, а также существование разных типов атомов во Вселенной, крупномасштабную стабильность вещества и ее основную массу.
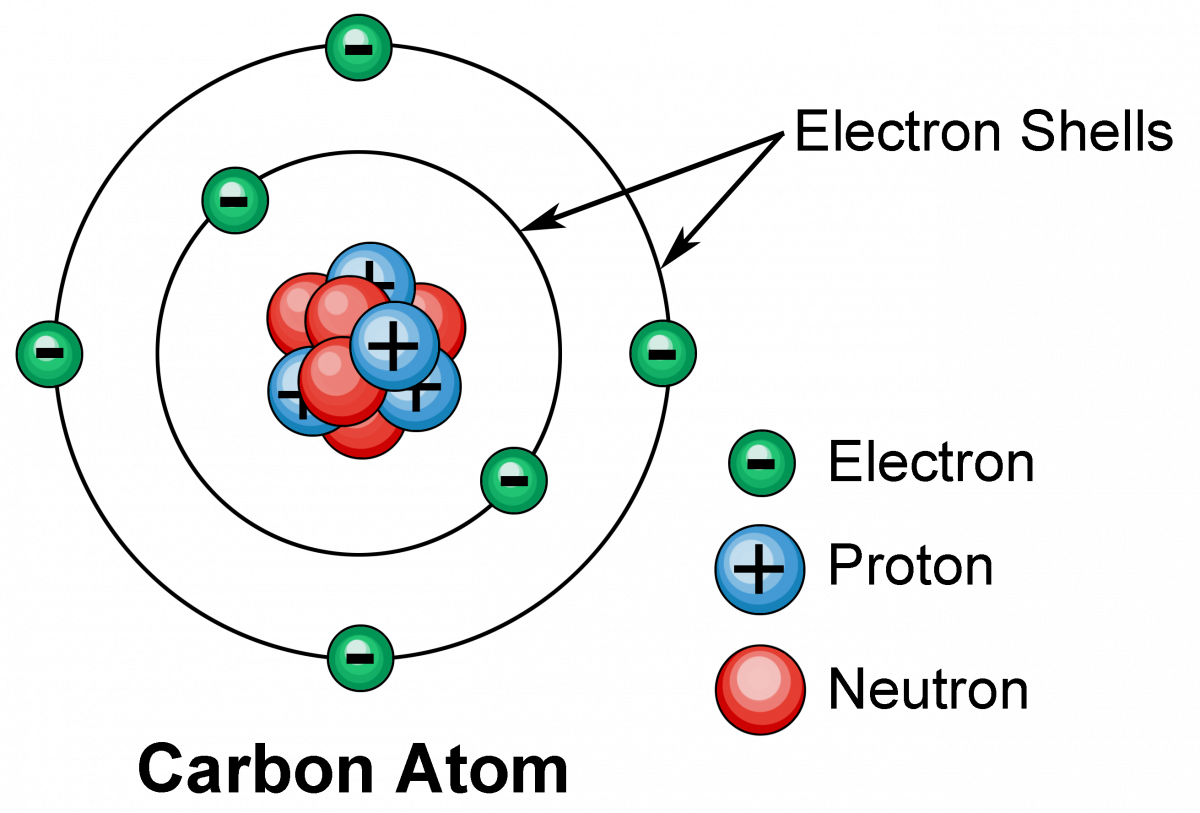
Чтобы понять важность этого принципа, необходимо знать, что, согласно боровской модели атома, электроны в атоме (существующие в том же количестве, что и протоны в ядре конкретного атома, чтобы общий заряд равнялся нулю) могут занимать только конкретные дискретные орбитальные позиции вокруг ядра, что также называют оболочкой атома. Чем ближе электроны к ядру, тем сильнее электрическая сила притягивает электрон внутрь и тем больше энергии понадобится, чтобы «вырвать» его из лап ядра. На самых близких к ядру орбиталях могут поместиться всего два электрона — один с верхним спином, а один — с нижним, чтобы иметь разные квантовые состояния. Оболочка энергетическим уровнем выше может вместить уже восемь, на уровень выше — 18, на следующем уровне — 32.
Принцип исключения Паули диктует, как электроны могут расположиться внутри атома по его орбиталям. Тот факт, что два электрона не могут одновременно занимать одно и то же квантовое состояние, не дает им «нагромождаться» друг на друга, тем самым объясняя, почему материя занимает исключительно свое место и не позволяет другим материальным объектам проходить через себя, но в то же время позволяет проходить через себя свету и излучению.
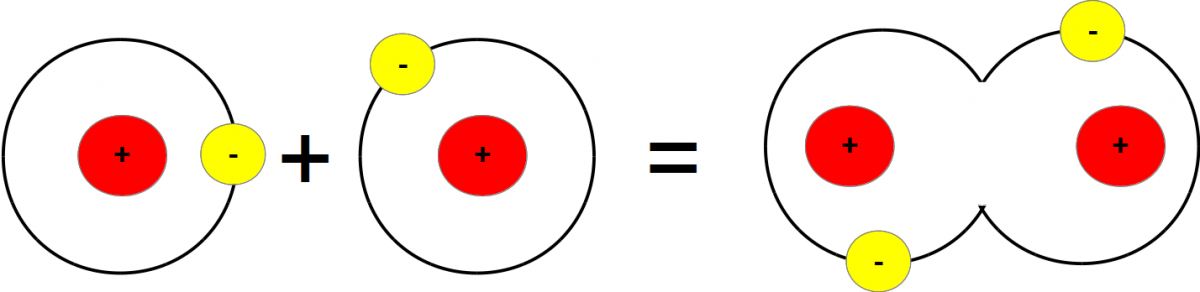
Этот принцип также объясняет существование разных атомов в периодической таблице и разнообразие мира, окружающего нас. Например, когда атом получает новый электрон, он всегда попадает на самый низкий из доступных энергетических уровней (наиболее отдаленную от ядра орбиталь). Два атома с «закрытыми» оболочками не могут осуществить химическую связь друг с другом из-за того, что электроны одного атома не находят доступных квантовых состояний, которые они могли бы занять в другом атоме. Итак, порядок электронов, а именно — электронов на самой отдаленной орбитали, также влияет на химические свойства элемента и способность атомов ко взаимодействию с другими атомами, а значит, и на то, как взаимодействуют молекулы при формировании газов, жидкостей или твердых тел, и на то, как они объединяются в живых организмах.
Принцип исключения Паули — один и самых важных принципов в квантовой физике, по большей части из-за того, что все три типа частиц, из которых состоит вся обычная материя (электроны, протоны и нейтроны), подчиняются ему. Однако интересно, что этот принцип не поддерживается никакими физическими силами, известными науке. Когда электрон входит в ион, он каким-то образом уже «знает» квантовые числа электронов, находящихся там, то есть знает, какие атомные орбитали он может занять, а какие — нет.
Американские биотехнологи впервые сообщили об обращении вспять клеточного старения в живых клетках печени человека — не мышиных, не синтетических, а именно человеческих. На волне этого результата компания привлекла 435 миллионов долларов и готовится к клиническим испытаниям.
Роль личности в истории чаще всего иллюстрируют правителями или полководцами. Но, глядя на современную карту мира, нельзя не признать: она выглядела бы принципиально иначе, если бы не одна крестьянская девушка, которую сожгли в этот день ровно 595 лет назад.
Старший преподаватель кафедры физики и технической механики РТУ МИРЭА Николай Зенченко проанализировал принципы работы одежды с маркировкой UPF — технологии, которая блокирует до 98% ультрафиолетового излучения. В отличие от солнцезащитного крема, такая защита не смывается водой и действует весь день, но при этом требует правильного выбора материала. Эксперт развеял популярные мифы: почему мокрая хлопковая футболка не спасает от ожогов, можно ли загореть в UPF-купальнике и зачем горнолыжной куртке защита от солнца.
В 2017 году человечество впервые заметило объект, прилетевший из другой звездной системы. Он оказался странным, почти не похожим ни на астероид, ни на комету, и получил имя Оумуамуа. Затем появился «нормальный» межзвездный странник — комета Борисова. А в 2025-м астрономы обнаружили 3I/ATLAS — объект, который, вероятно, хранит вещество времен рождения чужих миров. Но что изменили в астрономии эти три гостя из межзвездной тьмы?
Астрономы провели длительную радиодиагностику межзвездного объекта 3I/ATLAS и не нашли признаков искусственных технологий. Наблюдение окончательно подтвердило естественную природу ледяного тела, хотя ученые изначально не ожидали сенсации.
Тысячу лет назад колоссальный степной пояс от Амура до Дуная назывался Великой степью. На Руси его знали как Дикую степь. В этом краю жили кочевники, и среди них — хищная птица сокол-балобан. Сейчас цельной трансконтинентальной популяции балобана больше нет. Небольшой европейский островок уцелел в Венгрии, Австрии и в Крыму. Есть популяция в Казахстане, Монголии и Китае. В России сокол-балобан, помимо Крыма, живет в горах Южной Сибири. И выживание этой популяции, как и всего вида, под угрозой. Как живет эта птица и как ей помогают в нашей стране? Зачем в Хакасии посреди «нигде» построили огромный облёточник? Буквально сегодня в него уже доставили первую партию птиц.
В высокогорных районах Гималаев появился новый хищник. Он не боится людей, возглавляет стаи собак и все чаще заходит в деревни. Местные жители называют его «кхипшанг». Речь идет о гибриде гималайского волка и бродячей собаки. Ученые опасаются, что этот зверь изменит хрупкий баланс местной дикой природы и в скором времени станет весьма опасным для человека.
В доколумбовых Андах принадлежность к правящему роду определяла доступ к земле, торговле и статусу, поэтому удержать все внутри семьи было вопросом выживания. Ученые выяснили, что элиты долины Чинча решали эту задачу самым прямым способом — заключая браки между родственниками на протяжении как минимум двух поколений.
При совпадении нескольких условий наши глаза способны улавливать излучение в ближнем инфракрасном спектре. Тогда сетчатка начинает работать как нелинейный фотодетектор.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно






Последние комментарии