Уведомления
Авторизуйтесь или зарегистрируйтесь, чтобы оценивать материалы, создавать записи и писать комментарии.
Авторизуясь, вы соглашаетесь с правилами пользования сайтом и даете согласие на обработку персональных данных.
Клеточная алхимия
Колдуны и волшебники древности и во сне не могли помыслить о том, на что в действительности способны современные технологии «клеточной алхимии».
В 2012 году Нобелевская премия в области медицины и физиологии досталась авторам двух, пожалуй, самых важных открытий со времен расшифровки структуры ДНК. Эксперименты, проведенные японцем Синъей Яманакой (Shinya Yamanaka) и британцем Джоном Гёрдоном (John Gurdon) почти за полвека до вручения премии, сделали возможным то, что многие специалисты называют «клеточной алхимией». Ученые показали, что созревание стволовых клеток, их дифференциацию ? превращение в высокоспециализированные клетки организма ? можно обратить вспять. И запустить снова, в нужном нам направлении.
Со времен Левенгука, впервые рассмотревшего ранние стадии эмбриогенеза под увеличительным стеклом, ученые поражались удивительной гармоничности и сложности процесса, в результате которого оплодотворенная яйцеклетка превращается в сложный многоклеточный организм. Самая первая клетка ? зигота ? делится надвое, эти две превращаются в четыре, и так далее. И даже когда дело доходит до миллиардов клеток, каждая из них прекрасно знает, когда и каким образом ей делиться, где ее место и каково предназначение ? и развивается с поразительной согласованностью.
Синъя Яманака и Джон Гёрдон
©Kyodo/ Reuters
В конце XIX века появилась гипотеза, согласно которой в разных дочерних клетках накапливается разный наследственный материал, который и определяет направление ее развития и дифференциации. Эта идея, казалось бы, подтвердилась, когда известный немецкий анатом Вильгельм Ру (Wilhelm Roux), разделив пополам имевшего всего две клетки зародыша лягушки, вырастил из них два «полузародыша». Однако вскоре его соотечественник Ханс Дриш (Hans Driesch), экспериментируя с иглокожими, получил из двух разделенных клеток два совершенно одинаковых и совершенно полноценных организма. Вскоре к тому же результату привели опыты с 8-клеточными бластомерами тритона. Выходило, что, по крайней мере, на этом этапе развития делящиеся клетки эмбриона совершенно идентичны и несут одинаковый генетический материал.
Кстати, Ханс Шпеман (Hans Spemann), рассекавший зародыши тритона с помощью тонкого волоса, позаимствованного у собственной дочери, впервые и озвучил фантастическую по тем временам возможность переноса содержащего наследственность ядра из зрелой, высокоспециализированной клетки в яйцеклетку – с тем, чтобы проверить, превратится ли она в такую же зрелую клетку, или будет развиваться по пути обычного эмбриона. Несколько десятилетий спустя ? в 1950-х ? такой эксперимент был проведен с зародышем лягушки.
Ханс Дриш (Hans Driesch), экспериментируя с иглокожими, получил из двух разделенных клеток два совершенно одинаковых и совершенно полноценных организма
©EMSL
Из клетки, находившейся на стадии бластулы и уже начавшей дифференцироваться, удалось выделить ядро и перенести его в очищенную от собственной ДНК яйцеклетку. Действительно, такая клеточная химера вырастала во вполне нормальную и благополучно плававшую лягушку. Однако когда аналогичные попытки были предприняты с клетками более зрелыми и дифференцированными, число успешно выросших лягушек резко сократилось, ну а из клеток взрослого эндотелия получались лишь мертвые эмбрионы с глубоко нарушенным развитием. Эти результаты позволили предположить, что клетки, взрослея и специализируясь, постепенно теряют возможность развиваться по пути нормального эмбриона.
Тут на сцене появляется один из будущих лауреатов ? англичанин Джон Гёрдон, который провел тысячи экспериментов по переносу клеточного ядра на зародышах шпорцевых лягушек. В целом он подтвердил предыдущие выводы: эффективность развития нормальных эмбрионов падает по мере созревания клеток-доноров клеточного ядра. Важнее здесь то, что это правило на некоторых клетках не работало: несмотря на высоко дифференцированную стадию развития, они странным образом сохраняли способность снова давать рождение совершенно нормальным организмам. Получается, что все клетки не только несут идентичный генетический материал, но и их созревание не включает каких-то совершенно необратимых процессов, и каким-то способом может быть обращено вспять.
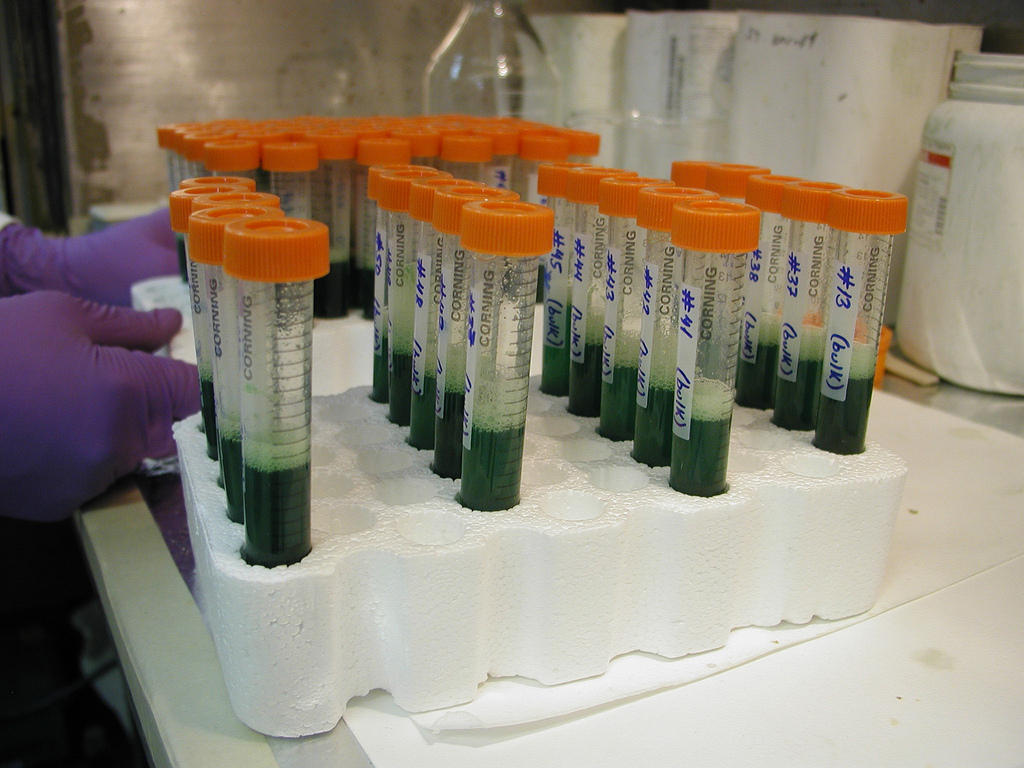
Извлечение ДНК
©CIMMYT
Опыты Гёрдона стимулировали целое направление экспериментальных работ по переносу ДНК из взрослых организмов в яйцеклетки ? тому, что сейчас принято называть клонированием. В 1983 году эта задача была впервые успешно решена на мышах (с более чем 90% благополучно выросших особей), однако ядра выделялись снова из клеток зиготы, а не взрослого организма. Со «взрослыми» клетками млекопитающих это не удавалось раз за разом, настолько, что авторы экспериментов в конце концов объявили эту задачу принципиально невыполнимой.
По счастью, не все к ним прислушались, и в 1996 году такие попытки увенчались появлением на свет успешно клонированной Долли, для которой ДНК была выделена из зрелой клетки молочной железы овцы. А годом спустя Джейме Томсону (Jamie Thomson) с коллегами удался следующий прорыв ? разработка методов культивирования в лаборатории недифференцированных эмбриональных стволовых клеток человека (hESC).
Дело оставалось за главным: соединить эти два достижения и научиться выращивать человеческие клетки. Если мы, например, возьмем ДНК из клеток человека, пораженных каким-нибудь генетическим заболеванием, то сможем вырастить с их помощью «взрослую» высокоспециализированную ткань, на которой это заболевание можно детально исследовать, учиться восстанавливать повреждения. Или, скажем, взяв здоровые клетки больного, выращивать из них новую ткань для трансплантации. Или даже превращать их в целые органы, готовые к пересадке…
Овца Долли — первое теплокровное животное-клон
©wikimedia
Первые успешные попытки проделать это были предприняты, однако, на лабораторных мышах с врожденным иммунодефицитом. Взяв такую клетку, ученые «в пробирке» скорректировали нарушения в ее геноме, затем стимулировали ее развитие в гемопоэтические стволовые клетки ? предшественницы клеток крови ? и благополучно «привили» их больным грызунам. Те продемонстрировали частичное восстановление нормального производства В- и Т-лимфоцитов, а следом ? и некоторое возвращение здорового иммунитета. Аналогичные результаты были получены с выращиванием из стволовых клеток «вылеченных» дофаминэргических нейронов и пересадкой их мышам с болезнью Паркинсона.
К сожалению, все эти работы были исключительно разовыми проектами, крайне сложными, многоступенчатыми, дорогостоящими и доступными лишь избранным лабораториям. При этом в обществе поднялась волна страхов за возможное «клонирование человека», о чем ученые до поры вообще-то и не заикались. Тем не менее, в США при Джордже Буше финансирование ряда направлений, связанных с hESC, было жестко ограничено, законодательные ограничения появились и в других странах. Отдельные ограничения, разумеется, касались работы с человеческими яйцеклетками ? все это могло резко замедлить развитие технологий и исследований.
Однако ключевые выводы уже были сделаны. Во-первых, стало точно известно, что все соматические (неполовые) клетки взрослого организма несут одинаковый геном. Во-вторых, стало понятно, что в цитоплазме клетки имеются все необходимые молекулярные системы для того, чтобы не только превращать ее в ту или иную специализированную клетку, но и ? при использовании точно выверенного набора химических сигналов ? возвращать ее в исходное состояние. Это состояние, из которого клетка может затем развиться практически в любую взрослую форму, называется плюрипотентным, а сам процесс изменения специализации клетки ? ее перепрограммированием.
В 2004 году в обзоре «Первые полвека ядерной трансплантации» Гёрдон писал: «Мы уверены, что способность яйцеклетки к перепрограммированию рано или поздно будет расшифрована на уровне конкретных молекул, и эти механизмы удастся использовать для перепрограммирования соматических клеток, которые удастся выращивать in vitro («в пробирке» ? NS)». Однако тогда задача выглядела невероятно трудной, и Гёрдон полагал, что еще лет 50 понадобится лишь для первого этапа работы ? понимания молекулярных механизмов, управляющих дифференциацией клеток.
Тем более весомыми оказались эксперименты, проведенные в лаборатории нашего второго лауреата ? японского профессора Синъи Яманаки. В начале 2000-х годов ученый исследовал участие ряда белковых факторов в возвращении клетки к плюрипотентной фазе (т.н. индуцированной плюрипотентности), а затем он поступил весьма остроумно. Вместо того, чтобы погружаться в детали работы бесчисленных регуляторных белков, ученый вспомнил, что, в конце концов, работа их должна обеспечивать изменения в активности каких-то конкретных генов ? и вскоре эти гены ему удалось выявить.
Синъя Яманака в лаборатории
©Chris Goodfellow
Нельзя сказать, что работа оказалась простой. Из многих сотен вариантов Яманака со своей командой отсеяли практически всех, и в итоге остановились на 24-х генах, участвующих в индуцировании плюрипотентного состояния. Воспользовавшись этим, ученые, наконец, сумели перепрограммировать мышиные фибробласты (клетки соединительной ткани), вернув их в юное плюрипотентное состояние. В конечном итоге Яманака остановился всего на четырех белках-факторах перепрограммирования, которые получили его имя. Вот этот список: Oct4, Sox2, KLF4 и c-Myc ? этого «магического зелья» «клеточным алхимикам» достаточно для того, чтобы вернуть взрослую соматическую клетку в раннее детство и получить из нее индуцированную плюрипотентную стволовую клетку (iPSC).
Вскоре к работе над iPSC подключилось множество исследовательских групп, и технологии их получения и дальнейших манипуляций стали быстро совершенствоваться. Буквально через год ? в 2007-м году ? были проведены первые успешные эксперименты по перепрограммированию человеческих клеток. Можно было переходить к практическому использованию этих результатов. Перепрограммирование позволило получить клеточные линии для исследования целого ряда сложных заболеваний ? болезни Паркинсона, различных форм иммунодефицита, диабета, рака. Сегодня «клеточная алхимия» развивается уже сотнями лабораторий по всему миру, где изучают болезни и способы их лечения, а наравне с тем ? и жизнь, и развитие здоровых клеток. На них можно проверить действие новых лекарственных препаратов, изучить эффекты радиации и генетической терапии. Из них выращивают ткани для пересадки ? и такие ткани организм больного никогда не отторгает, ведь выращены они из его собственных клеток. Делаются уверенные шаги по выращиванию целых органов для трансплантации. И если вскоре вместо того, чтобы пломбировать очередное дупло в зубе, мы сможем просто заказать себе новый, то это ? благодаря «клеточной алхимии».
Релиз довольно неожиданно перенес время образования протонов и нейтронов в более раннее прошлое Вселенной. К сожалению, из его текста осталось неясным научное обоснование таких фундаментальных изменений в космологии. Также он резко передвинул в прошлое и момент возникновения реликтового излучения.
Ученые, похоже, приблизились к разгадке происхождения пшеницы мягкой — той самой, из которой делают большую часть хлеба и другие мучные изделия. Согласно авторам нового исследования, она, предположительно, появилась 8000 лет назад на территории современной Грузии и Армении.
Обломки, найденные на дне Кадисского залива, оказались потопленным Фрэнсисом Дрейком торговым судном
Ученые смогли установить, что обломки затонувшего корабля, обнаруженные на морском дне возле испанского города Кадис, принадлежали генуэзскому торговому судну. Его потопили в 1587 году, во время налета на город английской эскадры под командованием Фрэнсиса Дрейка.
Поставщик элементов окололунной станции попытался сдать клиентам изделия, подвергшиеся коррозии еще до начала его монтажа. Об этом заявил новый глава NASA Джаред Айзекман. Защищая свою позицию, поставщик сообщил, что ранее он поставлял модули с коррозией для МКС, но они все равно до сих пор работают. NASA использует скандал для отказа от алогичного проекта Lunar Gateway, обитаемой космической станции на окололунной орбите.
Релиз довольно неожиданно перенес время образования протонов и нейтронов в более раннее прошлое Вселенной. К сожалению, из его текста осталось неясным научное обоснование таких фундаментальных изменений в космологии. Также он резко передвинул в прошлое и момент возникновения реликтового излучения.
Ученые, похоже, приблизились к разгадке происхождения пшеницы мягкой — той самой, из которой делают большую часть хлеба и другие мучные изделия. Согласно авторам нового исследования, она, предположительно, появилась 8000 лет назад на территории современной Грузии и Армении.
В последнее время пуски с российских северных космодромов осуществляют без предварительного уведомления, чего не было в прошлом. Вероятно, дело в недавно упомянутых главой «Роскосмоса» атаках на Плесецк во время пуска. Сегодняшний запуск обеспечил вывод на орбиту космических аппаратов военного назначения.
Когда международная экспедиционная группа, исследующая море Уэдделла в Антарктиде на борту ледокола «Поларштерн», попыталась укрыться от шторма, ученые и экипаж судна удивились внезапному появлению острова, не обозначенного ни на одной морской карте.
Окаменелые остатки рептилии возрастом 289 миллионов лет сохранили полное анатомическое устройство грудной клетки ранних покорителей суши. Благодаря нетронутым хрящам исследователи реконструировали механику первого полноценного реберного дыхания. Наличие в тканях оригинальных белков подтвердило, что сложные органические молекулы способны сохраняться в палеонтологической летописи почти на 100 миллионов лет дольше, чем считалось.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно












Последние комментарии