Ученые создали новую молекулу — альтернативу антибиотикам
Созданное соединение лишает болезнетворные бактерии защиты от иммунитета человека. При этом оно не затрагивает полезные микроорганизмы кишечника, открывая путь к новым методам борьбы с устойчивостью к антибиотикам.
Устойчивость бактерий к антибиотикам — серьезная проблема здравоохранения во всем мире. По оценкам Всемирной организации здравоохранения, ежегодно примерно пять миллионов человек умирают из-за инфекций, вызванных бактериями, которые не поддаются лечению существующими препаратами. Эксперты опасаются, что к 2050 году эта проблема может стать главной причиной смертей на планете.
Антибиотики значительно снизили смертность от инфекционных болезней, но их частое и не всегда оправданное применение привело к появлению устойчивых бактерий. К тому же антибиотики обычно действуют на жизненно важные процессы бактерий широкого спектра. Из-за этого они уничтожают не только вредные, но и полезные микроорганизмы, которые составляют микробиоту человека.
Это нарушает баланс микрофлоры и может привести к другим проблемам со здоровьем. Поэтому поиск новых мишеней в бактериальных клетках и разработка инновационных противоинфекционных средств — приоритетная научная и медицинская задача. Один из перспективных подходов — не убивать бактерии напрямую, а лишать их способности вызывать болезнь или приобретать устойчивость.
Международный консорциум ученых сосредоточился на белке Mfd (Mutation Frequency Decline). Он присутствует у многих бактерий, но отсутствует у человека и животных. Mfd помогает патогенам противостоять иммунной системе хозяина. Из-за этого белка могут появляться случайные мутации, которые повышают способность бактерий развивать устойчивость к лекарствам. Это делает Mfd привлекательной мишенью для новых препаратов.
Исследователи поставили задачу найти вещество, которое блокирует Mfd. С помощью компьютерного моделирования они проанализировали библиотеку почти из пяти миллионов молекул на способность связываться с активным центром Mfd — участком, где к белку присоединяется молекула АТФ, источник энергии для Mfd. Виртуальный скрининг выявил 95 перспективных кандидатов.
Последующие лабораторные тесты показали, что одна молекула, названная NM102, наиболее эффективно подавляет активность Mfd — на 85%. Дальнейшие эксперименты подтвердили, что NM102 соединяется именно с АТФ-связывающим участком белка Mfd и конкурирует с АТФ за это место. Сродство NM102 к Mfd оказалось даже выше, чем у самой АТФ. Проверка показала, что NM102 специфично действует на Mfd и не влияет на работу схожих АТФ-зависимых белков человека или других бактериальных белков.
Эффективность NM102 проверили на моделях инфекций у гусениц шелкопряда Bombyx eri и мышей. Молекула показала антимикробную активность только в условиях стресса, имитирующего иммунный ответ, например, при воздействии оксида азота NO, который производят иммунные клетки. В отсутствие такого стресса NM102 не влияла на бактерии.
NM102 значительно снижала в инфицированных органах количество патогенных бактерий, таких как Klebsiella pneumoniae и Pseudomonas aeruginosa, включая штаммы, устойчивые к антибиотикам. Например, у гусениц, зараженных P. aeruginosa, обработка NM102 снизила бактериальную нагрузку примерно в 300 раз.
Для удобства введения и повышения растворимости молекулу заключили в биоразлагаемые наночастицы из полимера PLGA. Дополнительные тесты на культурах клеток человека и на животных моделях показали отсутствие токсичности для организма хозяина.
Результаты, опубликованные в журнале Nature Communications, показали три ключевых эффекта NM102. Во-первых, молекула не убивает бактерии напрямую, а делает их уязвимыми для иммунной системы хозяина. Во-вторых, она снижает количество патогенов в организме, не нанося вреда полезной микробиоте — анализ состава кишечной микробиоты мышей не выявил значимых изменений после введения NM102.
В-третьих, NM102 блокирует механизм, который помогает бактериям вырабатывать устойчивость к лекарствам. Молекула подавляла способность Mfd ускорять мутации, снижая частоту возникновения устойчивости бактерий к антибиотикам рифампицину и стрептомицину в лабораторных условиях в восемь и два раза соответственно.
Открытие NM102 представляет собой новый подход к борьбе с инфекциями. Вместо прямого уничтожения бактерий предлагается стратегия их «разоружения», которая одновременно помогает иммунной системе справиться с патогеном и защищает полезную микробиоту. Способность NM102 снижать вероятность развития лекарственной устойчивости делает ее особенно перспективной.
Ученые уже запатентовали мишень — белок Mfd — и саму молекулу. Далее планируют оптимизировать NM102 и создать эффективные и безопасные лекарства на ее основе.
Долгое время считалось, что гигантские стрекозообразные, жившие 300 миллионов лет назад, стали такими из‑за высокого содержания кислорода. Тогда в атмосфере его было около 30% вместо сегодняшних 21%. Учёные полагали, что крупные насекомые задохнулись бы в нашей атмосфере. Но оказалось, что это не так.
Ученые давно сделали вывод о том, что в поздней Античности монеты перестали представлять собой цену как валюта, однако не было понятно когда именно это произошло. Новое исследование погребения римского воина из бельгийского форта Оденбург показало, в какой момент монеты стали цениться просто весом металла в кошельке.
Большой взрыв мог быть не началом Вселенной, а моментом рождения самой гравитации в привычном нам виде. Новая модель предлагает иную, квантовую форму гравитации, которая могла запустить инфляцию и избавить космологию от проблемы сингулярности, где законы физики перестают работать.
Релиз довольно неожиданно перенес время образования протонов и нейтронов в более раннее прошлое Вселенной. К сожалению, из его текста осталось неясным научное обоснование таких фундаментальных изменений в космологии. Также он резко передвинул в прошлое и момент возникновения реликтового излучения.
Поставщик элементов окололунной станции попытался сдать клиентам изделия, подвергшиеся коррозии еще до начала его монтажа. Об этом заявил новый глава NASA Джаред Айзекман. Защищая свою позицию, поставщик сообщил, что ранее он поставлял модули с коррозией для МКС, но они все равно до сих пор работают. NASA использует скандал для отказа от алогичного проекта Lunar Gateway, обитаемой космической станции на окололунной орбите.
Ученые, похоже, приблизились к разгадке происхождения пшеницы мягкой — той самой, из которой делают большую часть хлеба и другие мучные изделия. Согласно авторам нового исследования, она, предположительно, появилась 8000 лет назад на территории современной Грузии и Армении.
В последнее время пуски с российских северных космодромов осуществляют без предварительного уведомления, чего не было в прошлом. Вероятно, дело в недавно упомянутых главой «Роскосмоса» атаках на Плесецк во время пуска. Сегодняшний запуск обеспечил вывод на орбиту космических аппаратов военного назначения.
Четыре человека, летящие к Луне, столкнулись с целым рядом мелких неприятностей — от низкой температуры в начале работы до поломки мочевыводящей системы туалета на вторые сутки и необходимости взамен пользоваться пакетами. К счастью, пока самые крупные сложности удалось компенсировать. Но все они вместе могут сдвинуть ситуацию к решению, о котором Naked Science уже говорил в нашем видеоподкасте о миссии: не исключено, что при высадке астронавтов на Луне их корабль состыкуют со Starship не на окололунной, а уже на околоземной орбите.
Когда международная экспедиционная группа, исследующая море Уэдделла в Антарктиде на борту ледокола «Поларштерн», попыталась укрыться от шторма, ученые и экипаж судна удивились внезапному появлению острова, не обозначенного ни на одной морской карте.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно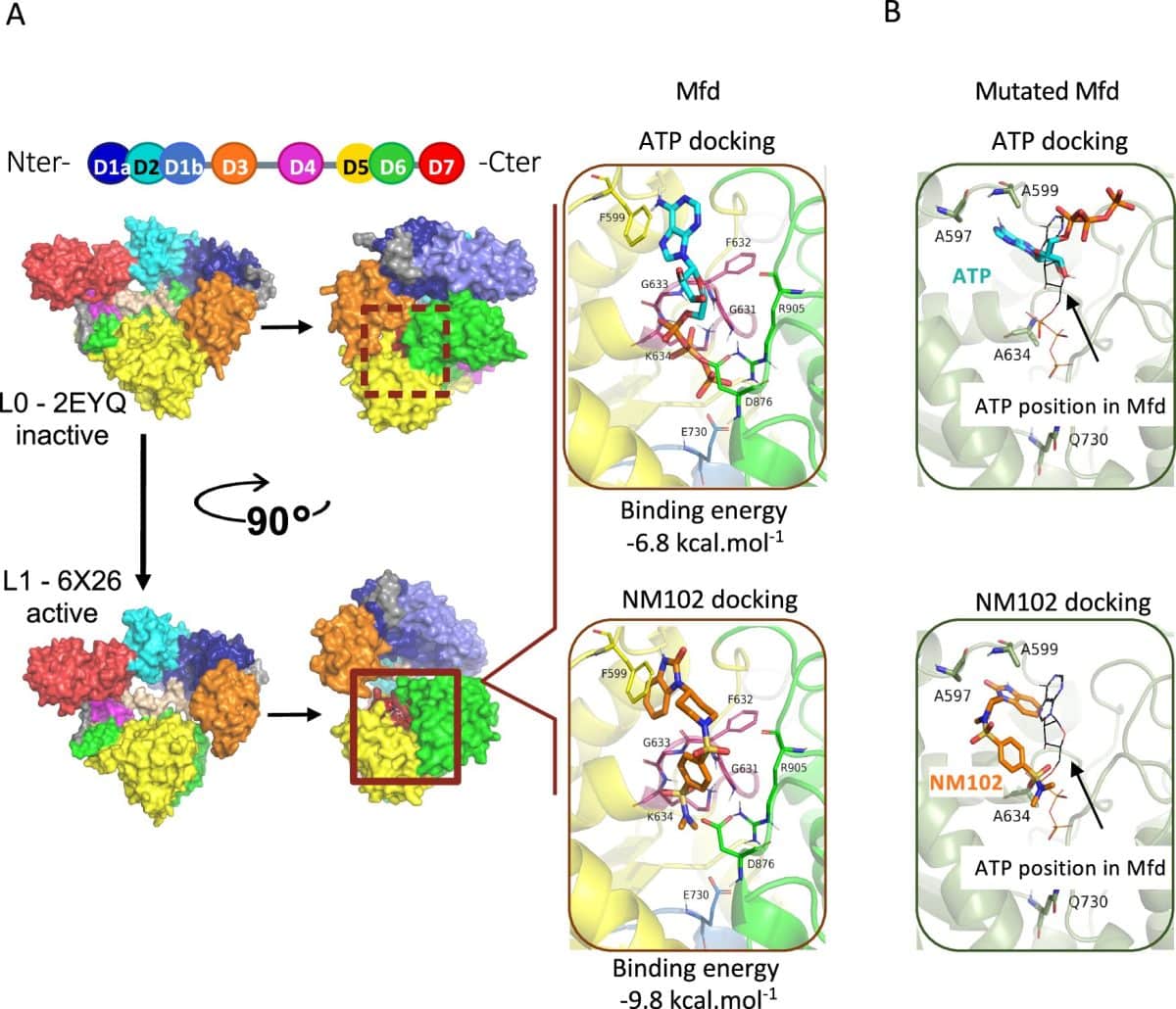









Последние комментарии