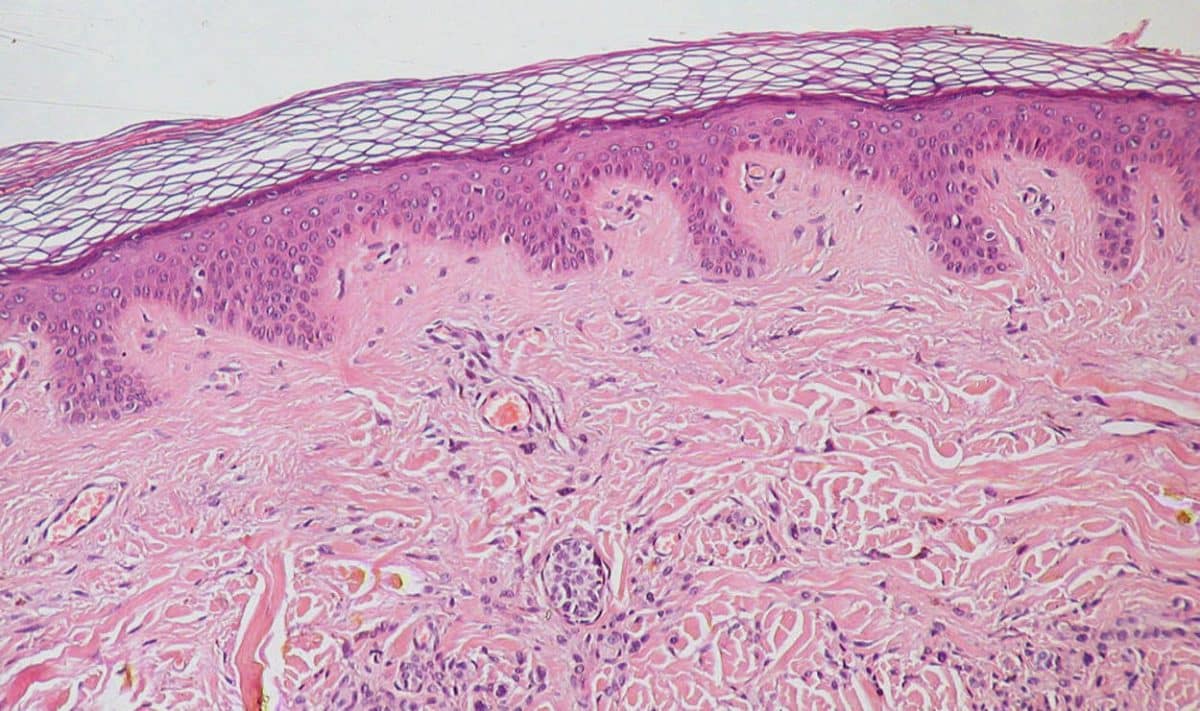
Ученые создали виртуальную модель эпителиальной ткани, способную прогнозировать развитие серьезных медицинских патологий
Способность организма к регенерации — сложный биологический процесс, при котором клетки координировано восстанавливают поврежденные ткани. Однако при различных патологиях эта система нарушается. У пациентов с диабетом возникают незаживающие язвы, после ожогов образуются рубцы, а при онкологии естественные механизмы клеточного деления и миграции приводят к метастазированию. Принципиально важно, что и нормальное заживление, и патологический рост опухоли управляются единым механизмом — движением эпителиальных клеток. Современные методы исследования ограничены: эксперименты в пробирке не отражают реальную сложность организма, врачи видят лишь конечные стадии болезней, а компьютерные модели либо игнорируют химические сигналы, либо используют упрощенные расчеты. Это мешает понять начальные этапы развития заболеваний. Ученые Пермского Политеха разработали алгоритм, который воспроизводит поведение живых тканей при порезах, ожогах, онкологических процессах — и прогнозирует их дальнейшее развитие.
Человеческий организм — сложнейшая система, и его основа — это ткани, состоящие из миллионов клеток. Его способность к регенерации после травм кажется нам чем-то само собой разумеющимся, однако на деле это сложнейший биологический механизм. Мы редко задумываемся, что за обычным заживлением раны (например, царапины) стоит целая совокупность слаженных реакций на микроуровне. Всего за несколько дней незаметные для глаза компоненты кожи успевают распознать повреждение, «согласовать» свои действия и полностью воссоздать утраченную биологическую структуру.
Однако иногда система дает серьезные сбои. При различных патологических состояниях естественные процессы восстановления выходят из строя, что приводит к тяжелым последствиям для организма. Например, у пациентов с сахарным диабетом, даже незначительная ссадина может трансформироваться в хроническую язву, которая не заживает месяцами. Это происходит из-за сбоя кровоснабжения тканевых структур и нарушения нервных окончаний.
Схожие проблемы возникают после обширных операций или термических ожогов, когда регенерация часто проходит тяжело и не без последствий. Вместо здоровой кожи может сформироваться грубый рубец, который не только создает косметический дефект, но и может ограничить подвижность суставов или нарушить функцию органов.
Однако наиболее опасное развитие событий наблюдается при онкологических заболеваниях, когда естественные процессы поведения структурных единиц начинают работать против организма. Запрограммированная природой способность биологических элементов к заживлению — их миграция и активное деление — превращается в смертельное оружие, приводящее к образованию метастазов — новым очагам опухоли. Они возникают в разных частях тела, и являются основной причиной гибели пациентов.
Как ни парадоксально, но и заживление ран, и рост опухоли управляются одним и тем же фундаментальным принципом — движением элементов эпителиальной ткани.
Чтобы научиться контролировать этот механизм, ученые применяют разные методы. Традиционно биологи наблюдают за клетками в пробирке, а врачи исследуют образцы уже развившихся опухолей у пациентов. Существуют и компьютерные модели, но они имеют недостатки: одни учитывают только физические свойства клеток, игнорируя химические сигналы, другие используют упрощенные расчеты и не могут точно описать изменение формы клеток при делении или движении. Все это создает ограничение таких подходов — они не способны полностью воспроизвести сложность живого организма, показывая лишь конечный результат болезни и упуская ее начальные и самые важные стадии развития.
Ученые Пермского Политеха создали уникальную компьютерную модель, в которой впервые учли механические и химические свойства каждой отдельной клетки. Она позволила воссоздать реальное поведение живых тканей при различных патологических состояниях — порезах, ожогах, онкологических процессах, а главное предсказать их последующие действия. Исследование опубликовано в «Российском журнале биомеханики» (том 29, №3, 2025).
Преимущество данной разработки в том, что она объединяет два важных принципа. Первый — это агентный подход, где каждая клетка способна вести себя как самостоятельный объект со своими свойствами. Второй — учет хемомеханических взаимодействий, то есть того, как химические сигналы организма влияют на физическое состояние структурного элемента и наоборот. Например, человек почувствовал запах еды (химический сигнал) и пошел на кухню (движение). И наоборот — когда он начинает жевать (механическое воздействие), во рту выделяется слюна (биохимическая реакция). Так же и клетки: биохимические сигналы заставляют их перемещаться, а физическое давление — менять внутриклеточные процессы.
Виртуальные биологические единицы ведут себя подобно живым: двигаются, делятся, меняют форму, взаимодействуют с «соседями», а также могут чувствовать сжатие, растяжение и даже «толкаться» друг с другом. Это похоже на то, как стая птиц синхронно меняет направление полета — каждая чувствует движение соседей и мгновенно подстраивается под общий поток, сохраняя расстояние и положение.
Чтобы проверить работоспособность цифрового аналога, исследователи воспроизвели «реальную» травму (порез), при которой мозг запускает механизм оповещения о повреждении. Результат превзошел ожидания: виртуальные клетки продемонстрировали скоординированное движение к источнику сигнала, полностью повторив естественный процесс регенерации тканей. Это подтвердило, что модель точно воспроизводит все принципы восстановления как в живых организмов.
— Наша внутренняя среда неоднородна — она содержит как жесткие (костные структуры, импланты), так и упругие границы (мышечная система, специальные биоматериалы). Исследования показали, что биологические элементы ведут себя совершенно по-разному в зависимости от типа окружающих препятствий. На жестких границах возникает зона максимального давления — клетки упираются в неподвижную преграду, формируя плотные скопления и опасные точки напряжения. В то же время упругие, податливые границы позволяют равномерно распределять нагрузку — клетки мягко отодвигают эластичные препятствия, снижая внутреннее давление и формируя более здоровую структуру, — поделился Иван Красняков, доцент, научный сотрудник кафедры «Прикладная физика» ПНИПУ, кандидат физико-математических наук.
Во время численного исследования исследователи выявили параметры поведения клеточных единиц. Ученые обнаружили, что существует «золотая середина», при которой сохраняется баланс между мобильностью и целенаправленным движением. При избыточной подвижности компоненты ткани теряют организованность.
— Деление клеток является одним из процессов, обусловливающих внутритканевую переупаковку (естественное изменение взаимного расположения клеток при делении, росте или восстановлении тканей). Когда структурные элементы перестают делиться, то возникают области с повышенным давлением. Тем самым нарушается естественное перераспределение нагрузки между соседними элементами. Без этого механизма физическое напряжение накапливается, как в переполненном офисе, где сотрудников меньше, а работы столько же. Это приводит к тяжелым последствиям: при диабете клетки кожи не могут закрывать раны, а в легких образуется рубцовая ткань вместо здоровой. Прекращение деления лишает ее главного инструмента саморегуляции, что постепенно разрушает структуру и функции, — рассказал Максим Бузмаков, младший научный сотрудник кафедры «Прикладная физика».
Особое значение также занимает энергетический баланс системы. Как показала модель, при нарушении деления биологических единиц энергия в клеточной системе распределяется неравномерно — в некоторых участках она достигает критических значений, что непосредственно связано с развитием патологий. Например, при фиброзе легких избыточная энергия в органах приводит к образованию плотных рубцов, а при хронических ранах у диабетиков нарушение энергетического баланса препятствует нормальному заживлению.
На практике, например, в онкологии предложенная модель будет работать следующим образом: у пациента берут образец биологического материала (гистологическую пробу), измеряют ключевые параметры клеток — их механические свойства, склонность к делению и миграции. Затем данные вводятся в систему, что позволяет воспроизвести индивидуальное развитие опухолевой ткани, спрогнозировать ее рост, потенциальное метастазирование и оценить эффективность различных терапевтических воздействий на течение болезни с помощью компьютерного моделирования — до их применения на пациенте.
Такой подход демонстрирует, что разработанная компьютерная платформа может применяться в широком спектре задач благодаря своей гибкости. Она открывает возможности для восстановительной медицины — от предсказания заживления ран до борьбы с раком. В онкологии модель может быть применима как инструмент помощи в принятии решений для лечащего врача, а в фармакологии — ускорить доклинические испытания препаратов. Большую ценность разработанная математическая методология имеет для персонализированной медицины: создавая цифровую копию ткани пациента, врачи смогут подбирать индивидуальное лечение для каждого человека.
В 2017 году человечество впервые заметило объект, прилетевший из другой звездной системы. Он оказался странным, почти не похожим ни на астероид, ни на комету, и получил имя Оумуамуа. Затем появился «нормальный» межзвездный странник — комета Борисова. А в 2025-м астрономы обнаружили 3I/ATLAS — объект, который, вероятно, хранит вещество времен рождения чужих миров. Но что изменили в астрономии эти три гостя из межзвездной тьмы?
Американские биотехнологи впервые сообщили об обращении вспять клеточного старения в живых клетках печени человека — не мышиных, не синтетических, а именно человеческих. На волне этого результата компания привлекла 435 миллионов долларов и готовится к клиническим испытаниям.
Роль личности в истории чаще всего иллюстрируют правителями или полководцами. Но, глядя на современную карту мира, нельзя не признать: она выглядела бы принципиально иначе, если бы не одна крестьянская девушка, которую сожгли в этот день ровно 595 лет назад.
В 2017 году человечество впервые заметило объект, прилетевший из другой звездной системы. Он оказался странным, почти не похожим ни на астероид, ни на комету, и получил имя Оумуамуа. Затем появился «нормальный» межзвездный странник — комета Борисова. А в 2025-м астрономы обнаружили 3I/ATLAS — объект, который, вероятно, хранит вещество времен рождения чужих миров. Но что изменили в астрономии эти три гостя из межзвездной тьмы?
Астрономы провели длительную радиодиагностику межзвездного объекта 3I/ATLAS и не нашли признаков искусственных технологий. Наблюдение окончательно подтвердило естественную природу ледяного тела, хотя ученые изначально не ожидали сенсации.
Роль личности в истории чаще всего иллюстрируют правителями или полководцами. Но, глядя на современную карту мира, нельзя не признать: она выглядела бы принципиально иначе, если бы не одна крестьянская девушка, которую сожгли в этот день ровно 595 лет назад.
В высокогорных районах Гималаев появился новый хищник. Он не боится людей, возглавляет стаи собак и все чаще заходит в деревни. Местные жители называют его «кхипшанг». Речь идет о гибриде гималайского волка и бродячей собаки. Ученые опасаются, что этот зверь изменит хрупкий баланс местной дикой природы и в скором времени станет весьма опасным для человека.
В доколумбовых Андах принадлежность к правящему роду определяла доступ к земле, торговле и статусу, поэтому удержать все внутри семьи было вопросом выживания. Ученые выяснили, что элиты долины Чинча решали эту задачу самым прямым способом — заключая браки между родственниками на протяжении как минимум двух поколений.
При совпадении нескольких условий наши глаза способны улавливать излучение в ближнем инфракрасном спектре. Тогда сетчатка начинает работать как нелинейный фотодетектор.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно