Микроскопу плоскостного освещения приделали автопилот
Американские ученые разработали программную платформу, которая позволяет автоматически настраивать фокус микроскопа плоскостного освещения в режиме реального времени. Результаты представлены в журнале Nature Biotechnology
Флуоресцентная микроскопия плоскостного освещения использует для получения изображения тонкий (408–1080 нанометров) фронт света. Фронт освещает часть образца, формируя его «срез», тогда как сам образец (расположенный «вертикально») может поворачиваться по горизонтальной оси. В сочетании с нефототоксичностью это позволяет ученым в объеме рассматривать отдельные клетки или целые организмы, например развивающиеся эмбрионы. В 2014 году технология была признана методом года по версии журнала Nature.
Главным недостатком «плоскостной» микроскопии является ручная фокусировка. Такие эксперименты требуют возможности наблюдать сложные клеточные изменения в течение часов и дней. Но даже успешная предварительная настройка разрешения не позволяет реконструировать образцы (особенно многоклеточные) по всем плоскостям с одинаковой детализацией: скорость изменений слишком высока. В результате даже несмотря на увеличение пространственного и временного разрешения применение метода остается ограниченным.
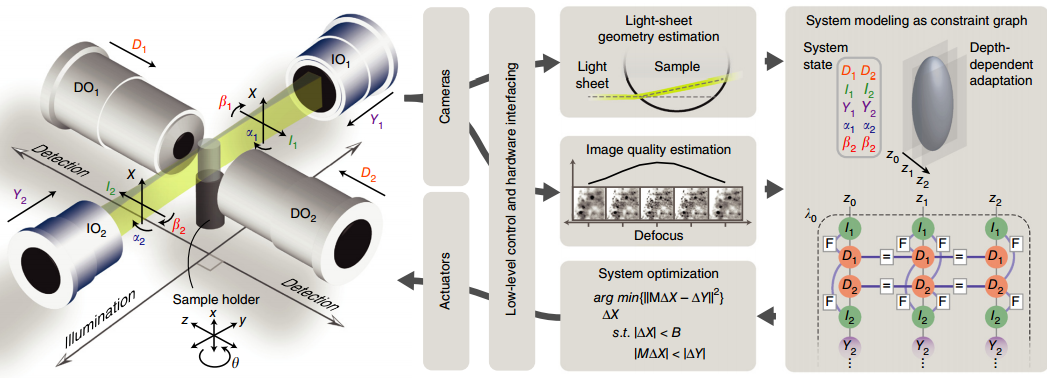
Для автоматизации процедур ученые из Медицинского института Говарда Хьюза разработали специальный фреймворк. В основу алгоритма легло сопоставление 30 параметров, которые характерны для тех или иных биологических моделей, с 66 наборами изображений из литературы и собственной базы данных. Конструкция микроскопа (авторы использовали SiMView, созданный в 2012 году) была изменена таким образом, чтобы одновременно с горизонтальным вращением образца фронт света мог перемещаться по «вертикальной» оси.
Каждая цилиндрическая линза при этом была оснащена парой гальванометрических сканеров. В ходе работы фреймворк управляет вращением образца и сканерами, и синхронизирует их движение с качеством изображения. Настройка разрешения осуществляется между точками сбора данных (каждые 375 миллисекунд) и заключается в том, что машина ищет наилучшую детализацию для «базовых» плоскостей, заданных пользователем (чаще это 4–8 граней с шагом в 20–80 микрометров). Таким образом, микроскоп может делать до шести «срезов» в трех измерениях по десяти степеням свободы с различной глубиной обнаружения (до 1,75 микрометра).
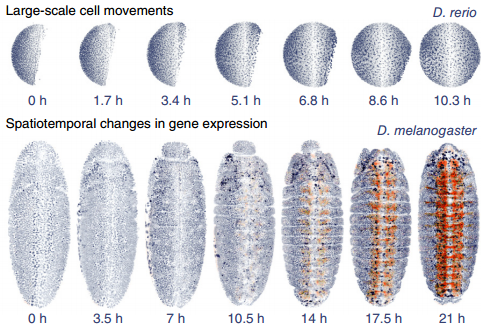
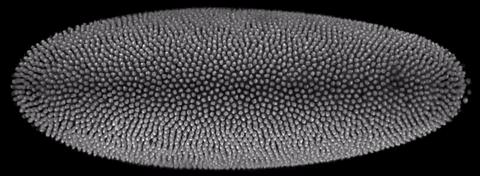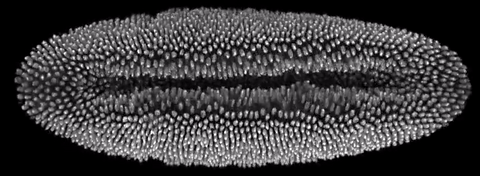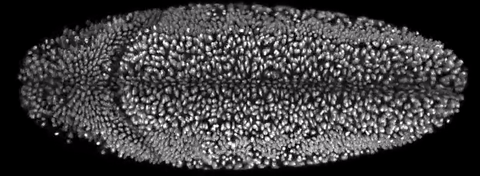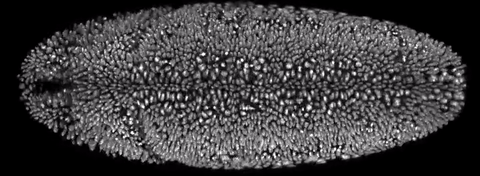
Система тестировалась на живых эмбрионах дрозофилы фруктовой (Drosophila melanogaster) и данио-рерио (Danio rerio). Результаты показали, что алгоритм позволяет отслеживать изменения в образцах (например, экспрессию белка) в течение 21 часа при потере около двух процентов данных. Первичная настройка параметров занимает около 40 секунд, после чего платформа в автоматическом режиме обрабатывает данные со скоростью один пиксель в 27 наносекунд. Средний рост пространственной разрешающей способности составил 2,4, временной — 1,6 (до 3 герц). Погрешность измерений оценивается в 330 микрометров.
«Мы хотели создать микроскоп настолько мощный и простой в использовании, насколько возможно. Фреймворк делает это, помогая пользователю убедиться в правильной настройке параметров и упрощая получение качественного изображения в каждом отдельном случае», — сообщил соавтор работы Филипп Келлер (Philipp Keller).
Платформа была написана на C++ и Java и управляется с помощью графического интерфейса. Скачать ее можно на странице проекта на GitHub.
Американские биотехнологи впервые сообщили об обращении вспять клеточного старения в живых клетках печени человека — не мышиных, не синтетических, а именно человеческих. На волне этого результата компания привлекла 435 миллионов долларов и готовится к клиническим испытаниям.
Роль личности в истории чаще всего иллюстрируют правителями или полководцами. Но, глядя на современную карту мира, нельзя не признать: она выглядела бы принципиально иначе, если бы не одна крестьянская девушка, которую сожгли в этот день ровно 595 лет назад.
В 2017 году человечество впервые заметило объект, прилетевший из другой звездной системы. Он оказался странным, почти не похожим ни на астероид, ни на комету, и получил имя Оумуамуа. Затем появился «нормальный» межзвездный странник — комета Борисова. А в 2025-м астрономы обнаружили 3I/ATLAS — объект, который, вероятно, хранит вещество времен рождения чужих миров. Но что изменили в астрономии эти три гостя из межзвездной тьмы?
В 2017 году человечество впервые заметило объект, прилетевший из другой звездной системы. Он оказался странным, почти не похожим ни на астероид, ни на комету, и получил имя Оумуамуа. Затем появился «нормальный» межзвездный странник — комета Борисова. А в 2025-м астрономы обнаружили 3I/ATLAS — объект, который, вероятно, хранит вещество времен рождения чужих миров. Но что изменили в астрономии эти три гостя из межзвездной тьмы?
Астрономы провели длительную радиодиагностику межзвездного объекта 3I/ATLAS и не нашли признаков искусственных технологий. Наблюдение окончательно подтвердило естественную природу ледяного тела, хотя ученые изначально не ожидали сенсации.
Тысячу лет назад колоссальный степной пояс от Амура до Дуная назывался Великой степью. На Руси его знали как Дикую степь. В этом краю жили кочевники, и среди них — хищная птица сокол-балобан. Сейчас цельной трансконтинентальной популяции балобана больше нет. Небольшой европейский островок уцелел в Венгрии, Австрии и в Крыму. Есть популяция в Казахстане, Монголии и Китае. В России сокол-балобан, помимо Крыма, живет в горах Южной Сибири. И выживание этой популяции, как и всего вида, под угрозой. Как живет эта птица и как ей помогают в нашей стране? Зачем в Хакасии посреди «нигде» построили огромный облёточник? Буквально сегодня в него уже доставили первую партию птиц.
В высокогорных районах Гималаев появился новый хищник. Он не боится людей, возглавляет стаи собак и все чаще заходит в деревни. Местные жители называют его «кхипшанг». Речь идет о гибриде гималайского волка и бродячей собаки. Ученые опасаются, что этот зверь изменит хрупкий баланс местной дикой природы и в скором времени станет весьма опасным для человека.
В доколумбовых Андах принадлежность к правящему роду определяла доступ к земле, торговле и статусу, поэтому удержать все внутри семьи было вопросом выживания. Ученые выяснили, что элиты долины Чинча решали эту задачу самым прямым способом — заключая браки между родственниками на протяжении как минимум двух поколений.
При совпадении нескольких условий наши глаза способны улавливать излучение в ближнем инфракрасном спектре. Тогда сетчатка начинает работать как нелинейный фотодетектор.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно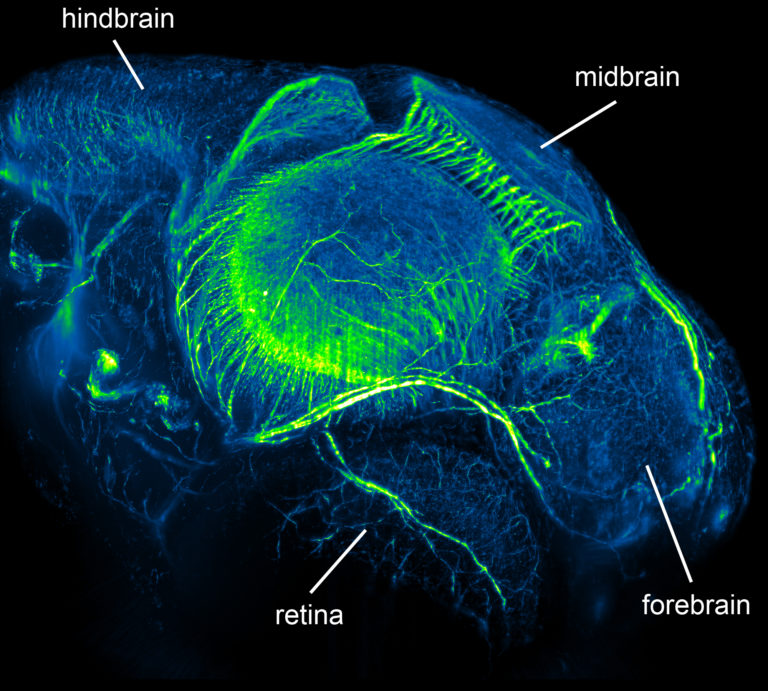








Последние комментарии