Уведомления
Авторизуйтесь или зарегистрируйтесь, чтобы оценивать материалы, создавать записи и писать комментарии.
Авторизуясь, вы соглашаетесь с правилами пользования сайтом и даете согласие на обработку персональных данных.
Цена омоложения: почему попытки обратить старение вспять повышают риск развития рака
Старение больше не кажется необратимым процессом: эпигенетические часы можно частично «отмотать» назад. Звучит здорово, но есть нюанс — вмешательство в программы клеточной идентичности затрагивает механизмы, которые эволюция выработала для защиты от рака. Получается парадокс: чем убедительнее работают методы омоложения, тем острее встает вопрос об их безопасности. Но действительно ли риск неизбежен?
Еще недавно старение описывали как односторонний биологический процесс. Эпигенетические метки — это химические знаки на ДНК, которые могут меняться под влиянием образа жизни, стресса и окружающей среды. С возрастом они постепенно смещаются, ткани теряют функции, а риск болезни Альцгеймера, сердечно-сосудистых и онкологических заболеваний растет. В целом концепция эпигенетических часов, предложенная более десяти лет назад, показала: возраст можно измерять по паттернам метилирования ДНК, а значит — теоретически и корректировать.
Исследования, опубликованные в журналах Cell и Nature Aging в феврале 2026 года, показали, что частичное перепрограммирование с помощью факторов Яманаки — набора белков, способных «перезапускать» генетическую программу клетки и возвращать ее в «юное» состояние, — может существенно омолодить клетки мозга и зрительной системы у старых лабораторных мышей.
Результаты оказались впечатляющими: факторы «включали» на короткое время, и биологический возраст тканей заметно снижался. При этом гены, ответственные за ремонт ДНК, начинали работать активнее, уменьшая воспаление, а нейроны — формировать новые связи. По итогу у пожилых мышей улучшились память и зрение.
Все это подкрепляет важную идею: старение — это не только накопление мутаций, но и постепенная потеря правильных «настроек» работы генов. Если эти настройки частично восстановить, клетки могут снова функционировать как молодые.
Однако именно здесь и возникает проблема. Даже без известного онкогена c-Мус вмешательство в эпигенетические программы может повышать риск развития рака. В ряде экспериментов у части зверьков спустя месяцы развивались глиомы — агрессивные опухоли мозга. При этом длительное или неконтролируемое включение факторов Яманаки может ослаблять естественные защитные барьеры организма.
Но если старение действительно можно обратить вспять, какую цену мы готовы за это заплатить?
Что такое эпигенетическое омоложение и факторы Яманаки
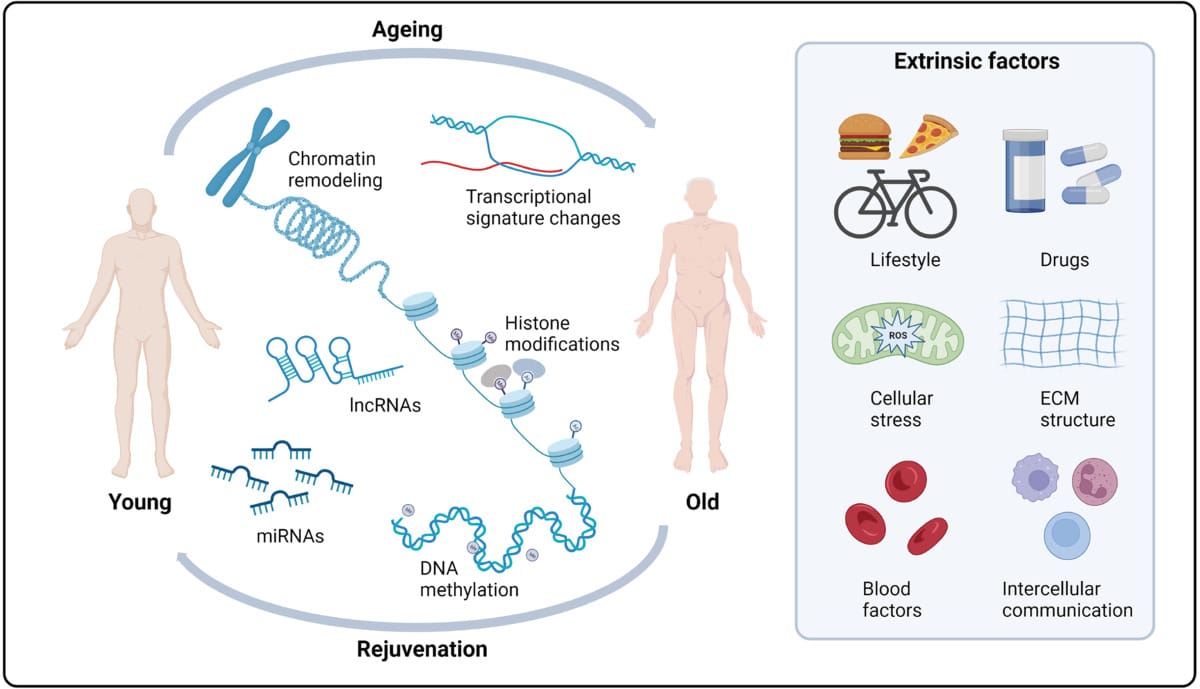
Как уже говорилось выше, эпигенетика не изменяет саму последовательность ДНК, а регулирует активность генов, определяя, какие будут выключены, а какие — включены. Ключевые механизмы здесь — метилирование ДНК, модификации гистонов (белков, вокруг которых «наматывается» ДНК) и ремоделирование хроматина — изменение упаковки ДНК за счет специальных белковых комплексов. Именно они формируют пространственную архитектуру генома и определяют, какие его участки будут доступны для транскрипции — процесса «считывания» информации из ДНК. Это первый шаг в реализации генетической программы.
С возрастом, однако, столь тонко настроенная система начинает «сбоить». Ученые называют это эпигенетическим дрейфом. Проще говоря, метки на ДНК постепенно смещаются: плотно закрытые участки генома приоткрываются, а нужные — наоборот, работают хуже. В результате включаются не те гены, а системы защиты и ремонта ДНК ослабевают: воспаление усиливается, повреждения хуже восстанавливаются, а ошибки — накапливаются. То есть она не разрушается в одночасье, а постепенно теряет четкость внутренних инструкций. Именно так старение проявляется на биологическом уровне.
Измерить этот процесс предложил биолог Стив Хорват (Steve Horvath) в 2013 году. Он создал так называемые эпигенетические часы — модель, которая оценивает возраст ткани по характерным химическим меткам на ДНК. Выяснилось, что биологический возраст может не совпадать с паспортным: у кого-то клетки стареют быстрее, а у кого-то — медленнее. И чем быстрее «тикают» эти часы, тем выше риск развития рака, диабета, болезней сердца и мозга. Это было важное открытие: если возраст можно измерить по молекулярным изменениям, стало быть, теоретически на них можно и повлиять.
Основа для такого вмешательства появилась еще в 2006 году. Тогда японский ученый Синъя Яманака (Shinya Yamanaka) показал, что если добавить в зрелую клетку четыре специальных белка (Oct4, Sox2, Klf4 и c-Myc), ее можно «перезапустить» и вернуть в состояние, похожее на эмбриональное. Такие клетки называют индуцированными стволовыми (iPSC). Они способны превращаться почти в любой тип клеток. Открытие стало революцией в биологии и принесло Яманаке Нобелевскую премию.

Правда, полное «обнуление» клетки оказалось слишком радикальным шагом для омоложения живого организма. Один из белков — c-Myc — связан с развитием рака. Более того, полная перезагрузка стирает клеточную память: клетка попросту забывает, кем она была и может начать бесконтрольно делиться: в опытах на животных это нередко приводило к образованию опухолей.
Поэтому ученые разработали более осторожный подход — частичное перепрограммирование. В нем используют только три фактора (без главного онкогена c-Myc): их включают ненадолго и под строгим контролем. Цель — не превратить клетку в эмбриональную, а лишь «освежить» ее состояние, немного восстановить молодые настройки, усилить механизмы ремонта и снизить воспаление. В ряде экспериментов подход омолаживал клетки по молекулярным показателям на десятки процентов, не стирая их идентичность.
При этом на молекулярном уровне клетки лучше справлялись со стрессом и повреждениями ДНК. Например, в опытах с повреждением зрительного нерва у взрослых животных наблюдалось восстановление волокон — то, что раньше считалось практически невозможным. В других моделях воспаление уменьшалось и частично утраченные функции тканей возвращались.
Сегодня интерес к технологии выходит за пределы лабораторий. Еще в 2018 году компания Rejuvenate Bio (с участием Дэвида Синклера и его команды) объявила о планах использовать частичное перепрограммирования для борьбы с возрастными изменениями у собак — с прицелом на то, что успешные результаты откроют путь для людей. Статья, опубликованная в журнале MIT Technology Review, назвала это «тихим стартапом Гарварда», который хочет обратить старение сначала у домашних животных, а потом, возможно, и у нас.
С тех пор прошло почти восемь лет. Сначала технологии проверяли на животных, затем — в ветеринарных испытаниях, а в будущем планируются первые эксперименты на людях. При этом ясно одно: эпигенетическое омоложение перестало быть просто теорией — теперь это реальный инструмент, позволяющий вмешиваться в базовые механизмы старения, а значит, и в системы, защищающие нас от рака.
Что именно произошло в последних экспериментах
В начале этого года на сервере препринтов Корнеллского университета вышла работа, в которой ученые работали не с отдельными клетками в пробирке, а со старыми мышами, внимательно отслеживая, как вмешательство влияет на ткани на молекулярном уровне и работу органов в целом.
Для этого исследователи применили метод частичного перепрограммирования с тремя факторами Яманаки (Oct4, Sox2, Klf4, OSK). Ключевым элементом эксперимента стала транзиторная активация: OSK включали всего на несколько недель, а затем гены омоложения отключали. Подход позволил «откатить» возраст клеток, не превращая их в эмбриональные и не стирая идентичность. В эксперименте участвовали десятки зверьков, разделенных на контрольные группы и группы с дополнительными мерами по контролю иммунного ответа, чтобы оценить как эффективность, так и возможные побочные эффекты.
Результаты показали, что слой нервных волокон сетчатки увеличился на 25-30 процентов, свидетельствуя о частичном восстановлении ее структуры. Более того, нейроны начали формировать новые связи — явление крайне необычное для взрослых млекопитающих.
Эпигенетический возраст тканей снизился на 30-50 процентов, показывая реальное молекулярное омоложение. Гены, ответственные за восстановление ДНК, активизировались, как и повышение устойчивости к стрессу и антиоксидантной защите. В то же время воспаление в тканях уменьшилось, в том числе в мозге — на десятки процентов. В моделях повреждений зрительного нерва наблюдалось восстановление волокон, а в тестах на память и ориентированность в пространстве животные были быстрее контрольной группы.

Частичное эпигенетическое омоложение действительно улучшило работу старых клеток и тканей. Причем эффект проявляется не только в нервной системе: предыдущие эксперименты на сердце, почках и других органах показали, что OSK помогает восстанавливать функции различных тканей, хотя нервная система реагирует особенно чувствительно.
Анализ активности также выявил сотни генов, связанных с репарацией ДНК, защитой клеток и метаболической регуляцией, при этом программы старения и воспаления подавлялись. То есть речь идет о системной перенастройке работы клетки, а не только о локальных изменениях отдельных генов.
Эффективность такого омоложения, однако, была сопряжена с риском: даже без c-Myc вмешательство повышало вероятность развития опухолей. Напомним, в предыдущих экспериментах у части животных формировались глиомы и другие виды рака. Это показывает, что частичное омоложение на уровне работы генов и клеточных процессов может ослабить встроенные защитные механизмы, сдерживающие неконтролируемое деление клеток.
Таким образом, омолодить ткани можно, но этот метод несет в себе потенциальную угрозу, превращая технологию из перспективной идеи в предмет серьезного биологического, клинического и этического обсуждения.
Риски и побочные эффекты: почему омоложение может убить
Ряд исследователей полагает, что частичное перепрограммирование может быть безопасным, если исключить один из наиболее онкогенных факторов — c-Myc. На деле это не так: даже без его вмешательства в настройки, в клетках может запуститься программа деления, которая в норме помогает организму развиваться или восстанавливаться, но при сбое теоретически способна приводить к опухолям.
В тканях, где клетки почти не делятся — например, в зрелых нейронах, риск ниже. Проблема в том, что мозг состоит не только из них. Есть глиальные клетки — вспомогательные клетки нервной ткани (астроциты и микроглия), которые делятся и поддерживают работу нейронов. Именно они чаще всего страдают от «сброса» эпигенетических часов и могут превратиться в опухолевые, однако прямых данных о массовой трансформации глии или ее частичном программировании пока нет.
Дополнительный фактор риска связан со способом «доставки» генов. В экспериментах чаще всего используют относительно безопасные адено-ассоциированные вирусы — вирусные «переносчики» генов, которые почти не встраиваются в геном клетки. Но иногда это все-таки происходит рядом с генами, ответственными за контроль роста или защиту опухолей, из-за чего их работа нарушается. Вирусы, помимо прочего, вызывают иммунный ответ: молекулы, выделяющие маркеры воспаления, рассматриваются учеными как потенциальный фактор риска.
Поскольку вмешательство затрагивает здоровые ткани, а не больные клетки, проблема усугубляется. Даже кратковременное воспаление в мозге может изменить среду и ослабить контроль деления глиальных клеток. Вот почему комбинация эпигенетической нестабильности и воспаления — известный «рецепт» для развития рака.
Еще один немаловажный аспект — это длительность наблюдений. Большинство экспериментов с частичным перепрограммированием длится 6-12 месяцев, а опухоли могут появляться только через год или два. То есть реальный риск онкологии, вероятно, выше, чем кажется.
Парадокс клеточного старения также имеет место. Старые клетки, которые перестают делиться, защищают организм, сигнализируя иммунной системе о необходимости их удаления. Теоретически частичное омоложение может вернуть им эту способность, однако ошибки в ДНК это не исправит. В результате в организме появляются опасные для здоровья молодые клетки с поврежденной генетикой.
До сих пор эксперименты с частичным перепрограммированием проводились в основном на мышах, а данных по долгосрочной безопасности у приматов и тем более людей практически нет. Вот почему отсутствие длительных наблюдений и ограниченность моделей остаются главным источником опасений среди ученых.
Следующая опасность связана с теломерами — своеобразными «колпачками» на концах хромосом, которые ограничивают число делений клетки. Вот только восстановить их с помощью частичного омоложения можно далеко не всегда. И хотя внешне модифицированные клетки выглядят здоровыми, их внутренний ресурс ограничен, что потенциально ускоряет старение других тканей.
В целом обзоры последних лет показали: риск развития опухолей, вероятно, зависит от множества факторов, времени экспрессии (то есть активности работы генов) и типа ткани. Особенно уязвимыми считаются мозг и печень. Выходит, эпигенетическое омоложение — это не просто обновление клеток, а вмешательство в самые фундаментальные механизмы контроля роста, защиты от онкологии и стабильности ДНК. И пока мы не научились четко отделять омоложение от рака, каждое вмешательство остается экспериментом с потенциально смертельным концом.
При этом сама по себе высокая скорость деления клеток не означает неизбежность развития онкологии. В организме есть ткани, которые обновляются чрезвычайно быстро и сравнительно редко становятся источниками рака. Например, эпителий тонкого кишечника полностью обновляется за 3-5 дней — и тем не менее частота злокачественных новообразований в этих тканях относительно невысока.
В толстом кишечнике, напротив, скорость клеточного обновления ниже, но рак там встречается гораздо чаще. Это означает, что решающим фактором может быть не само деление, а эффективность механизмов поддержания геномной стабильности, контроля и иммунного надзора. Следовательно, в теории эпигенетическая терапия не обязана автоматически сопровождаться ростом онкологических рисков — все зависит от того, насколько точно сохраняются системы противоопухолевой защиты.
Также нельзя исключать, что дальнейший поиск конкретных механизмов работы такой системы защиты позволит ученым и «омолаживать» те или иные клетки, и не рисковать при этом ростом вероятности рака.
Контраргументы и альтернативные подходы
Другие исследовательские группы напротив, не считают частичное эпигенетическое перепрограммирование приговором. По их мнению, это технология, которая находится в процессе «взросления». Проблема же заключается в том, как именно ее применяют: если подобрать правильную «дозу» факторов Яманаки, строго контролировать время их работы и направлять только в конкретные цели, риск превращения клеток в опухолевые может снизиться.
При использовании OSK факторы включают короткими импульсами с длительными паузами, что позволяет клеткам стабилизироваться. В тех же экспериментах на мышах подход восстанавливал функции зрительного нерва без развития рака. Именно этот аргумент приводят противники смертельного исхода генной модификации, называя ее потенциальной терапией болезни Альцгеймера и глаукомы.
Компании, работающие с этой технологией, активно разрабатывают меры безопасности, используя алгоритмы машинного обучения — последние анализируют изменения в генах и эпигеноме до и после вмешательства. Также появляются такие системы доставки, как тканеспецифичные промоторы (выключатели для генов, которые работают только в определенных типах клеток), самоуничтожающиеся вирусные векторы и CRISPR-подобные решения, активирующие программы омоложения организма (хоть и ненадолго).
Критики, впрочем, напоминают: даже при идеальном контроле концепция остается рискованной. Клеточное старение — сложный процесс, который останавливает деление и защищает организм от рака. Если такие клетки омолодить, не убрав ошибки, риски появления опухолей возрастут.
Кроме того, старение включает эпигенетические изменения, накопление мутаций, хроническое воспаление, укорочение теломер и истощение стволовых клеток. Поскольку частичное перепрограммирование влияет в основном на эпигенетический слой, а другие проблемы оставляет нетронутыми, это делает подход мощным, но не универсальным инструментом.
На этом фоне развиваются более «мягкие» альтернативы. Комбинация сенолитиков — препаратов, убирающих стареющие клетки — с дазатинибом и кверцетином, снижает воспаление и улучшает физическое здоровье пожилых людей без признаков повышенной онкогенности в краткосрочных испытаниях. Следовательно, метаболическая коррекция снижает биологический возраст, а сами препараты переносятся хорошо.
Существуют более экспериментальные методы: миметики калорийной рестрикции (препараты, имитирующие «эффект диеты»), терапия теломеразой и поддержка стволовых клеток без глобального перепрограммирования. Они, как правило, оказывают скромный эффект, но несут меньший риск для клеточной идентичности.
Выбор стратегии — это спор о балансе между эффективностью и безопасностью. Да, можно пойти радикальным путем, переписывая клеточную память с риском онкологии, но лучше делать все постепенно, используя безопасный комбинированный подход. Ну а будущее биомедицины зависит от того, какой баланс окажется приемлемым для науки, клинических испытаний и общества.
Этика, доступность и будущее
Когда технологии частичного перепрограммирования покинут стены лабораторий, возникнет вопрос: кто сможет ими пользоваться и влетит ли это в копеечку? Сегодня эксперименты обходятся в миллионы долларов на пациента, что делает их доступными лишь для богатых людей и крупных медицинских центров. Ранее история генной терапии показала — дорогие методы усиливают глобальное неравенство.
Если омоложение действительно продлит активную жизнь на десятилетия, разрыв между теми, кто сможет обнулить биологический возраст, и теми, кто нет, станет экономическим и демографическим. По сути, появится форма социального разделения по биологическому возрасту, что поднимает еще более сложный вопрос: должны ли такие технологии быть элитной услугой или общественным благом?
Особую тревогу вызывают последствия для будущих поколений, поскольку эпигенетические метки могут частично передаваться потомству. Хотя данных у ученых немного, эксперименты на животных продемонстрировали, что вмешательства в эпигеном родителей иногда отражаются на потомстве, повышая риск развития целого ряда заболеваний. То есть улучшая жизнь одного поколения, мы теоретически повлияем на биологию следующего — без их согласия.

Этические дискуссии также подчеркивают необходимость прозрачности данных, долгосрочных наблюдений и строгого информированного согласия. Внимание также следует уделить вопросу системного омоложения, когда вмешательство затрагивает весь организм, включая половые клетки. В США регуляторы уже сталкиваются с дилеммой: считать ли это лечением конкретных болезней или вмешательством в естественный процесс старения.
Все сложно и с «дизайнерским» старением — если перепрограммирование улучшает когнитивные способности, регенерацию и метаболизм, появится соблазн использовать технологию для «улучшения» человека. В конечном итоге граница между медициной и биотехнологической «прокачкой» станет размытой. В то же время доступность таких технологий, вероятно, возрастет: массовое производство векторов и стандартизация протоколов могут привести к снижению стоимости услуг.
Развитие, по мнению ученых, будет поэтапным. В ближайшие годы можно ожидать клинических испытаний локальных вмешательств — например, для лечения болезней мозга или глаз. Международные инициативы по здоровому старению также подчеркивают значимость равного доступа к новым технологиям: неконтролируемые процедуры «на стороне» могут привести к осложнениям, в том числе онкологическим, что подорвет доверие к науке.
Будущее эпигенетического омоложения зависит в том числе от того, сможет ли общество найти баланс между инновациями, безопасностью и справедливым распределением ресурсов.
Россия в контексте глобального тренда
В нашей стране исследования в области эпигенетики активно ведутся, но пока что в основном на фундаментальном уровне. Российские ученые изучают ключевые механизмы старения — дрейф метилирования ДНК (постепенное смещение химических меток на генах), модификации гистонов — белков, вокруг которых упакован генетический материал, — а также работу эпигенетических часов — моделей, позволяющих оценивать биологический возраст тканей. Такие работы помогают понять, какие гены включаются и выключаются с возрастом, и как это влияет на функции клеток и тканей.
Например, в 2022 году в Институте цитологии РАН применили эпигенетические часы для оценки старения тканей матки. Подход позволил измерить ее биологический возраст на молекулярном уровне, что стало важным шагом на пути к пониманию тканеспецифического старения — то есть того, как именно и на какой скорости стареют ткани и органы. Такие исследования закладывают основу для точной оценки возраста конкретной ткани, что позволит целенаправленно ее омолаживать.
В других научных центрах страны, а также в Институте общей генетики имени Н.И. Вавилова изучают эпигенетические маркеры возрастных болезней, включая онкологию и нейродегенерацию. Специалисты ищут изменения в метилировании ДНК, связанные с болезнью Альцгеймера и предрасположенностью к сердечно-сосудистым и метаболическим заболеваниям. Эти маркеры могут помочь в ранней диагностике и подборе персонализированных стратегий замедления старения.
При этом в России пока нет клинических программ по частичному перепрограммированию с факторами Яманаки (OSK), но фундаментальные исследования идут полным ходом. В 2025-2026 годах биологи участвовали в международных проектах по сенолитикам и эпигенетическим биомаркерам старения, что позволило интегрировать отечественные данные в глобальную научную картину.
Кроме того, в рамках национальных программ «Новые технологии сбережения здоровья» (2026-2030) планируется создание тест-систем для оценки биологического возраста тканей и органов. Эти системы могут лечь в основу будущей локальной терапии, где омоложение будет происходить путем минимизации риска побочных эффектов.

Интересно, что тема омоложения обсуждалась и на высоком политическом уровне. В 2025 году в рамках двусторонней встречи китайского лидера Си Цзиньпина и президента России Владимира Путина говорилось о перспективах таких технологий и их влиянии на здоровье населения. Особое внимание спикеры обратили на необходимость безопасного внедрения инноваций и международного сотрудничества.
Как и на Западе, этическим и социальным вопросам отечественные исследователи уделяют много внимания: понимание того, что технологии омоложения могут быть дорогостоящими, заставляет задуматься о равном доступе к инновациям. Причем, вопрос не только в науке, но и во внедрении технологий на пользу общества, а не только элиты.
Таким образом, Россия не стоит в стороне от мирового тренда, активно строя фундамент для клинических исследований и решений социальных и этических вопросов. Ну а ключевой вывод остается универсальным: как сделать будущие технологии омоложения доступными, безопасными и справедливыми для всех.
Будущее, которое мы выбираем
В 2026 году стало ясно: факторы Яманаки умеют не только перепрограммировать клетки в пробирке, но и частично отматывать назад биологический возраст живых тканей. Так, у мышей эпигенетический возраст снижался, пластичность нейронов восстанавливалась, а память и ориентация в пространстве — улучшились. Вместе с тем в некоторых случаях появлялись опухоли. Этот двойной результат — омоложение и риск развития рака — стал своеобразным символом эпохи: мы вплотную приблизились к управлению старением, но пока не умеем полностью контролировать последствия.
Строго говоря, это не конец старения и не «рецепт бессмертия», а начало новой главы в истории медицины, где старение перестает быть неизбежностью и рассматривается как процесс, который можно изменить. Эпигенетика показала: возраст — это не только износ, но и «информационная программа» клетки, которую можно переписать. Однако любое вмешательство затрагивает глубинные процессы: контроль деления клеток, защиту от опухолей и баланс иммунной системы.
Именно по этой причине ученые работают осторожно, применяя циклическое и органно-специфическое включение факторов. Они также комбинируют частичное перепрограммирование с сенолитиками для оценки рисков. Будущее, вероятно, за комбинированными стратегиями, где омоложение станет лишь одним инструментом наряду с корректировкой метаболизма, иммунной модуляцией и точечной генетической терапией.
Сегодня эта технология остается «на грани»: она обещает революцию в лечении нейродегенеративных и возрастных заболеваний, но в то же время напоминает об опасности любого вмешательства. Дело в том, что каждая попытка ускорить восстановление клеток может вывести их из-под контроля.
Отсюда следует, что все зависит не только от точности научных данных, но и от зрелости систем регуляции и выбора общественности. Станет ли частичное перепрограммирование безопасной терапией или останется осторожным лабораторным инструментом — покажут грядущие десятилетия.
Релиз довольно неожиданно перенес время образования протонов и нейтронов в более раннее прошлое Вселенной. К сожалению, из его текста осталось неясным научное обоснование таких фундаментальных изменений в космологии. Также он резко передвинул в прошлое и момент возникновения реликтового излучения.
На границе возможностей оптоволокна лазерный пучок самоорганизовывается в мощный, сфокусированный луч-иглу. Параметры этого излучения таковы, что позволяют в реальном времени без дополнительных ухищрений рассматривать клеточные процессы.
Поставщик элементов окололунной станции попытался сдать клиентам изделия, подвергшиеся коррозии еще до начала его монтажа. Об этом заявил новый глава NASA Джаред Айзекман. Защищая свою позицию, поставщик сообщил, что ранее он поставлял модули с коррозией для МКС, но они все равно до сих пор работают. NASA использует скандал для отказа от алогичного проекта Lunar Gateway, обитаемой космической станции на окололунной орбите.
В последнее время пуски с российских северных космодромов осуществляют без предварительного уведомления, чего не было в прошлом. Вероятно, дело в недавно упомянутых главой «Роскосмоса» атаках на Плесецк во время пуска. Сегодняшний запуск обеспечил вывод на орбиту космических аппаратов военного назначения.
Палеонтологи описали новый вид хищного клопа из мелового периода, передние лапы которого эволюционировали в клешни-пинцеты. Подобная анатомическая трансформация стала лишь четвертым задокументированным случаем за всю историю насекомых. Ископаемый вид получил название в честь корейской поп-группы Stray Kids из-за характерного положения застывших в смоле конечностей.
Спустя два с половиной года после того, как подводный аппарат обнаружил на дне залива Аляска загадочный «золотой шар», ученым, наконец, удалось разобраться в природе этого объекта. Они пришли к выводу, что это отброшенная часть оболочки или основания гигантской глубоководной актинии.
В последнее время пуски с российских северных космодромов осуществляют без предварительного уведомления, чего не было в прошлом. Вероятно, дело в недавно упомянутых главой «Роскосмоса» атаках на Плесецк во время пуска. Сегодняшний запуск обеспечил вывод на орбиту космических аппаратов военного назначения.
Четыре человека, летящие к Луне, столкнулись с целым рядом мелких неприятностей — от низкой температуры в начале работы до поломки мочевыводящей системы туалета на вторые сутки и необходимости взамен пользоваться пакетами. К счастью, пока самые крупные сложности удалось компенсировать. Но все они вместе могут сдвинуть ситуацию к решению, о котором Naked Science уже говорил в нашем видеоподкасте о миссии: не исключено, что при высадке астронавтов на Луне их корабль состыкуют со Starship не на окололунной, а уже на околоземной орбите.
Когда международная экспедиционная группа, исследующая море Уэдделла в Антарктиде на борту ледокола «Поларштерн», попыталась укрыться от шторма, ученые и экипаж судна удивились внезапному появлению острова, не обозначенного ни на одной морской карте.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно








Последние комментарии