Праймированное редактирование ДНК прошло клинические испытания на людях
Мы уже писали про праймированное редактирование в 2019 году. Тогда гарвардские ученые придумали технологию, которая, по их оценкам, способна исправить почти 89% известных врожденных мутаций человека. Спустя семь лет метод не только доказал свою пригодность, но и впервые вошел в клинику, пройдя испытания на людях. Хотя путь и оказался сложнее, чем предполагалось.
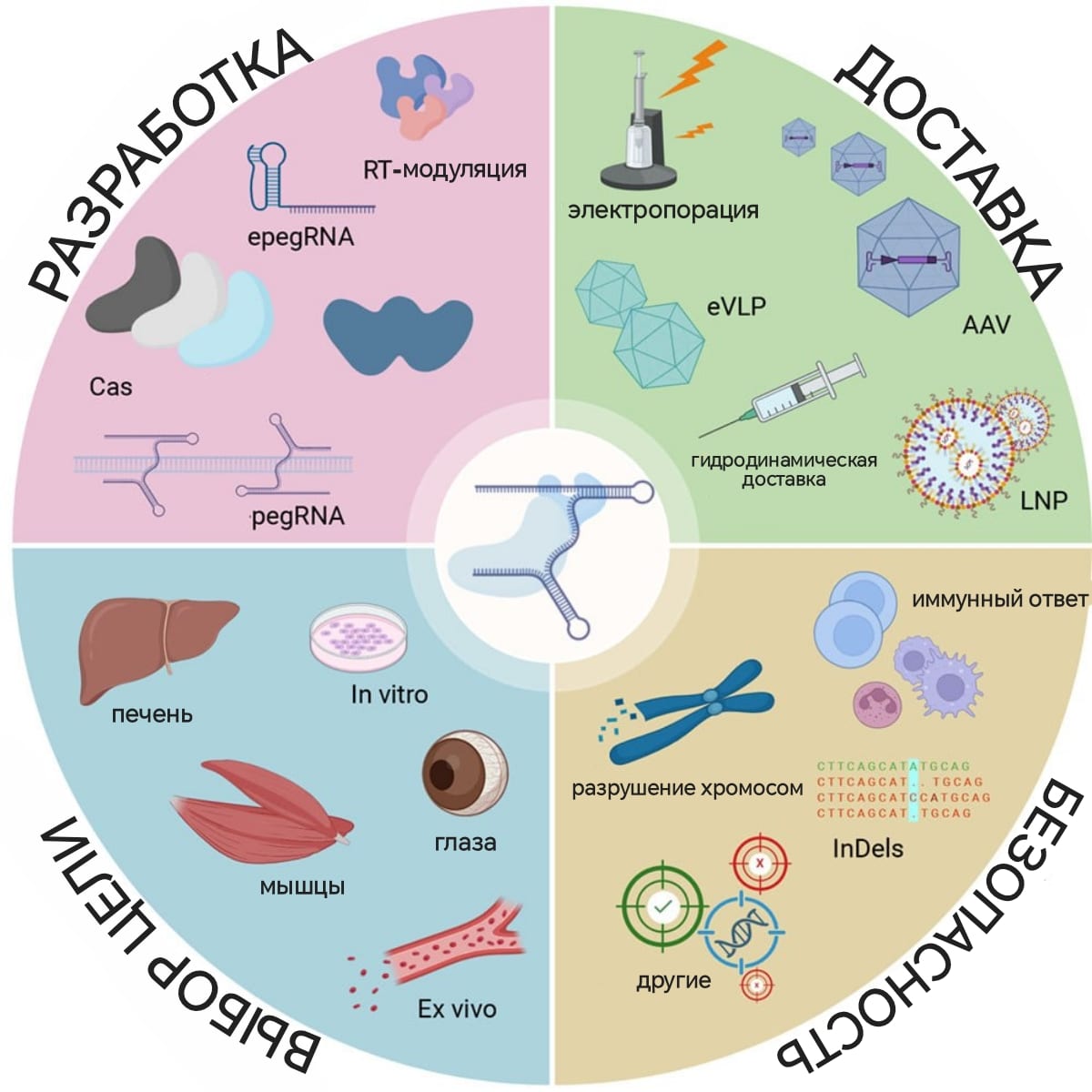
Классический CRISPR-Cas9 — это молекулярные «ножницы», режущие обе нити ДНК в заданном месте, после чего клетка пытается залатать разрыв. Но часто случаются ошибки: случайно удаляются или вставляются генетические «буквы». Поэтому такой метод не подходит для исправления конкретной мутации. В 2019 году ученые предложили праймированное редактирование: они взяли «испорченный» Cas9, режущий только одну нить из двух, и прикрепили к нему обратную транскриптазу. Этот инструмент позволяет создавать новую цепочку ДНК, используя РНК как готовую «инструкцию по сборке». А еще они придумали гибридную pegRNA, что не только наводит Cas9 на цель, но и несет в себе черновик нужной правки.
То есть Cas9 делает надрез одной цепи ДНК, освободившийся конец находит на pegRNA нужный участок и обратная транскриптаза дописывает новый фрагмент прямо в разрыв. В итоге праймированное редактирование позволяет аккуратно добавлять или удалять конкретные участки генетической информации, работая только с одной нитью ДНК и становясь своеобразным «текстовым редактором». Однако на практике возникли проблемы с эффективностью и доставкой.
Столкнувшись с низкой эффективностью метода в разных клетках, ученые провели ряд изменений. Оказалось, что один из концов цепочки pegRNA (ее «хвост») быстро «съедают» клеточные нуклеазы — «молекулярные уборщики», которые умеют разрезать цепочки ДНК и РНК на части. Поэтому на «хвост» был добавлен защитный псевдоузел epegRNA. Позже добавили также белок La, который защищает РНК от деградации, и так получили систему праймированного редактирования ДНК под названием PE7. Методом непрерывной эволюции при помощи фагов (PACE) нашли более компактные и активные версии обратной транскриптазы, и появились варианты PE6a, PE6b, которые намного меньше исходных, — это важно для упаковки в вирусные векторы (вирусы, переносящие такие «биологические ножницы»).
Главный «враг» технологии праймированного редактирования — система репарации неспаренных оснований (MMR). Это «служба контроля качества», которая следит, чтобы в ДНК организма не было ошибок и «опечаток», ведущих к раку и другим проблемам. Она же распознает несовпадения в ДНК, возникающие при редактировании, и отменяет правку. С помощью доминантно-негативного белка MLH1 ее научились подавлять, также увеличивая эффективность. Затем задумались о расширении мишеней для новой технологии, поэтому теперь подход может нацелиться почти на любую позицию в геноме.
И это еще не все. Если оригинальная версия была хороша для замены 1-3 «букв», то теперь возможно, например, вставить целый ген. Для этого стали использовать двойные pegRNA, использующие две направляющие вместо одной. Они синтезируют комплементарные цепочки с разных сторон дефекта, которые сшиваются вместе. Так можно вырезать кусок ДНК размером до десяти тысяч пар оснований (PRIME-Del) или, наоборот, вставить фрагмент.
Отдельная головная боль — доставка. Стандартные аденоассоциированные вирусы (AAV) вмещают не более 4,7 тысячи пар оснований, тогда как для полноразмерного праймированного редактированиятребуется около 6,3 тысячи пар оснований, не говоря о дополнительных архитектурах. Нашли несколько решений этой проблемы. Так, белок можно разрезать на две половины, чтобы каждую упаковать в свой вирус, а потом сшить его внутри клетки. Так исправляли мышей с наследственной тирозинемией и с врождённой слепотой. Эффективность невысокая, но достаточная для клинического эффекта, так как исправленные клетки получают преимущество в росте.
Также можно использовать липидные наночастицы (LNP), которые применяют для вакцин на основе матричной РНК. В LNP можно упаковать матричную РНК белка-редактора и химически модифицированные pegRNA. В печени мыши удалось добиться 8% правки гена Pcsk9 — мишени для снижения холестерина. Но LNP естественно накапливаются в печени, значит, для мышц или мозга нужны другие подходы. Для доставки возможно использовать и вирусоподобные частицы (eVLPs), которые представляют из себя оболочку вируса с готовым внутри комплексом праймированного редактирования с РНК. В 2024 году такие eVLP доставили комплекс праймированного редактирования в сетчатку мыши и исправили мутацию, вызывающую слепоту, с эффективностью около 15%.
Но самый надежный способ пока — ex vivo, то есть забрать клетки у пациента, отредактировать их в пробирке и вернуть обратно. Именно так технология праймированного редактирования впервые добралась до человека. В 2025 году в New England Journal of Medicine вышла статья о двух пациентах с редким наследственным иммунодефицитом — хронической гранулематозной болезнью (ХГБ). У них была мутация delGT в гене NCF1, из-за чего их нейтрофилы не могли убивать бактерии. Врачи забрали у пациентов стволовые клетки крови (HSPC), отредактировали их ex vivo с помощью праймированного редактирования, а потом вернули обратно после лёгкого курса химиотерапии, чтобы освободить место в костном мозге.
В результате доля исправленных клеток в инфузионном продукте составила 13-23% (по GTGT-аллелям), а через месяц у второго пациента 83% нейтрофилов снова умели производить активные формы кислорода. Функция сохранялась через четыре и шесть месяцев наблюдения без серьёзных побочных эффектов, связанных с применением праймированного редактирования. То есть, первое in vivo применение на людях показало, что метод безопасен и функционально эффективен.
Можно ли в итоге исправить 89% вредных мутаций, как это было обещано разработчиками новой технологии в 2019 году? Технически — да, праймированное редактирование может нацелиться на большинство известных точечных мутаций, но «текстовый редактор» оказался капризным. Несмотря на это, технология добралась до пациентов, и уже готовятся следующие испытания: для серповидноклеточной анемии, для метахроматической лейкодистрофии, для муковисцидоза.
Ученые РТУ МИРЭА и Сибирского федерального университета создали программный комплекс, который анализирует учебные планы вузов быстрее секунды и находит в них слабые места. Большинство учебных планов содержат скрытые противоречия, дублирования и неочевидные перекосы в подготовке специалистов. Это важно, потому что от качества учебного плана напрямую зависит, какие реальные навыки получат студенты и насколько они будут востребованы работодателями.
В популярной литературе сверхмассивные черные дыры чаще всего представляют как разрушители звезд и планет. Авторы новой работы попробовали рассчитать, что на самом деле происходит в окрестностях таких объектов и пришли к противоположному выводу.
Значение вилочковой железы (тимуса) для здоровья и долголетия, возможно, сильно недооценивалось. Как показали результаты двух новых исследований, нормально функционирующий во взрослом возрасте тимус — залог здорового старения, долгой жизни и высокой выживаемости при раке.
Вначале Reuters опубликовал статью о взаимоотношениях SpaceX и Пентагона, которую миллиардер --- традиционно для его отношений с этим изданием — назвал фейком. Опровергая ее тезисы, он обнародовал информацию, не представленную ранее публично.
Исследователи опросили более 60 тысяч испытуемых из разных стран и выяснили: чем больше человек зациклен на себе, тем холоднее он к своему партнеру. Правда, снижение накала страстей не всегда плохо, у этого есть и положительные стороны.
Около четырех миллиардов лет назад Солнечная система пребывала в хаосе: гигантские планеты сближались, меняли орбиты и выбрасывали своих соседей в межзвездное пространство. Хотя шансы на «выживание» лун Юпитера и Урана в этот период были крайне малы, астрономы показали, что их судьба может хранить следы древней катастрофы с участием «потерянной» планеты.
В высокогорных районах Гималаев появился новый хищник. Он не боится людей, возглавляет стаи собак и все чаще заходит в деревни. Местные жители называют его «кхипшанг». Речь идет о гибриде гималайского волка и бродячей собаки. Ученые опасаются, что этот зверь изменит хрупкий баланс местной дикой природы и в скором времени станет весьма опасным для человека.
В доколумбовых Андах принадлежность к правящему роду определяла доступ к земле, торговле и статусу, поэтому удержать все внутри семьи было вопросом выживания. Ученые выяснили, что элиты долины Чинча решали эту задачу самым прямым способом — заключая браки между родственниками на протяжении как минимум двух поколений.
При совпадении нескольких условий наши глаза способны улавливать излучение в ближнем инфракрасном спектре. Тогда сетчатка начинает работать как нелинейный фотодетектор.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно








Последние комментарии