Ученым удалось разгадать механизм работы вирусного белка всего по трем процентам его «длины»
Исследователи Сколтеха и их коллеги из России, США и Швеции описали необычную РНК-полимеразу, транскрибирующую гены малоизученного crAss-подобного бактериофага. Ученым удалось «поймать» этот фермент, используя очень малую часть (составляющую менее трех процентов) аминокислотной последовательности, подобной другим РНК-полимеразам. Понимание механизма инфицирования хозяйских клеток этими фагами позволит контролировать состав микробиома, что, в свою очередь, важно для борьбы с различными заболеваниями.
Статья с подробным описанием этого открытия опубликована в журнале Nature. CrAss-подобные фаги – аналоги открытого недавно бактериофага crAssphage, который получил свое название от метода сборки генома (cross-assembly). Ученые обнаружили этот вирус, проводя исследование имеющихся в открытом доступе данных о метагеноме фекалий человека (метагеном представляет собой совокупность информации о генетически последовательностях всех микроорганизмов, присутствующих в образце).
Удивителен тот факт, что вирус crAssphage, обнаруженный только в 2014 году, оказался самым распространенным фагом в кишечной микрофлоре человека. Позднее ученые, в том числе соавтор этой статьи Евгений Кунин и его коллеги, обнаружили и других представителей этого класса вирусов, которые ранее никогда не исследовались в лабораторных условиях.
«Поскольку crAss-подобные фаги – самые распространенные вирусы в кишечнике человека, понимание механизма инфицирования хозяйских клеток этими фагами позволит контролировать состав микробиома, что, в свою очередь, важно для охраны здоровья человека и борьбы с различными заболеваниями. Наш интерес к изучению crAss-подобных фагов обусловлен еще и тем, что эти вирусы транскрибируют свои гены, используя необычные РНК-полимеразы (то есть ферменты, формирующие РНК на основе шаблона ДНК)», − отмечает старший преподаватель Центра наук о жизни Сколтеха (CLS) Мария Соколова.
Соколова и ее коллеги использовали crAss-подобный фаг phi14:2, который инфицирует бактерии Cellulophaga baltica, широко распространенные на побережьях. Оказалось, что этот вирус удобно использовать в качестве модели для лабораторных исследований. В частности, ученые исследовали предсказанную РНК-полимеразу этого вируса — gp66, представляющую собой достаточно крупный белок, функция которого ранее была неизвестна.
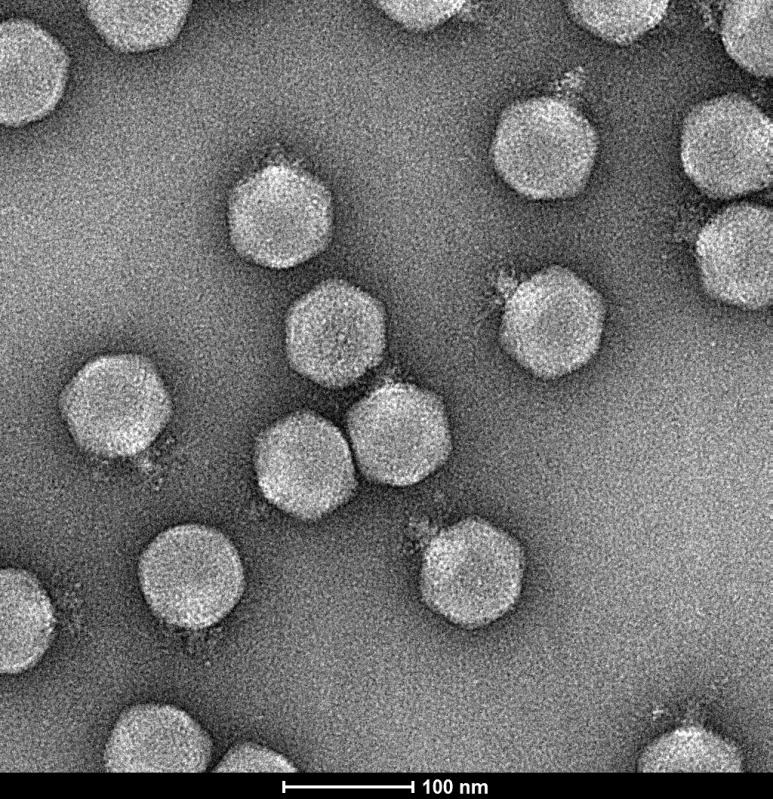
Анализируя аминокислотную последовательность gp66, исследователи обнаружили в ней небольшой фрагмент, напоминающий фрагмент клеточной мультисубъединичной РНК-полимеразы. Исследователи выделили белок gp66 и продемонстрировали in vitro, что он выполняет функцию РНК-полимеразы.
«Стандартный тест на активность РНК-полимеразы, который обычно дает положительный результат для всех других РНК-полимераз, показал, что предсказанная РНК-полимераза crAss-подобного фага является неактивной. Зная о наличии необычных свойств у ферментов вирусов, мы продолжили тесты в поиске активности и в итоге нашли ее. Мы были очень довольны полученным результатом, поскольку до этого момента мы сомневались в достоверности предсказаний с помощью методов биоинформатики, в которых сходство gp66 с известными ферментами оказывалось минимальным», − рассказывает Соколова.
В экспериментах in vitro было показано, что антибиотик рифампицин блокирует собственную РНК-полимеразу бактерии C. baltica, но не оказывает никакого воздействия на gp66. Исследователи проверили, какие гены phi14:2 в итоге транскрибируются в инфицированных клетках в присутствии рифампицина и обнаружили множество так называемых ранних генов, которые кодируют механизмы, необходимые вирусу для захвата хозяйской клетки на ранних стадиях инфекции.
При этом средние и поздние гены, проявляющие активность на более поздних стадиях инфекции, присутствовали в меньших количествах. Это говорит о том, что вирус phi14:2 обладает своей собственной РНК-полимеразой; белок gp66 он использует на ранней стадии инфекции, прежде чем сам сможет воспользоваться полимеразой хозяйской клетки.
Ученые не только смогли определить кристаллическую структуру белка gp66, но и обнаружили, что большинство его структурных элементов не имеет известных аналогов, а их функции неизвестны. Однако было установлено сходство центральной части gp66 с РНК-полимеразой, которая у высших организмов участвует в процессе РНК-интерференции, что позволяет подавлять функцию некоторых генов.
По словам соавтора статьи Константина Северинова, «это потрясающий результат, позволяющий предположить, что источником ферментов РНК-интерференции − процесса, который считался характерным лишь для клеток высших организмов (эукариот), является фаг. Другими словами, эти ферменты были «заимствованы» у бактериального вируса − предка современных crAss-подобных фагов на ранних этапах эволюции.
Это открытие показывает, что эволюция высших клеток представляла собой сложный процесс, в ходе которого происходили многократные приобретения предковыми клетками ферментов бактерий и даже фагов. Еще один классический пример этого процесса − приобретение целых бактерий предковой эукариотической клеткой, которая впоследствии стала митохондрией».
Исследователи также установили, что в кристаллической структуре gp66 каталитически активный центр находится в конформации, которая ранее никогда не наблюдалось ни в одной РНК-полимеразе. Ученые предположили, что до упаковки в фаговую частицу gp66 находится в выключенном состоянии. «Данный фермент обладает свойствами, характерными для белков, образующих оболочки вирусов (например, гемагглютинина, гликопротеинов флави- и альфавирусов). Эти белки проходят этап созревания во время сборки вирусных частиц, необходимый для обеспечения их активности.
У РНК-полимеразы сrAss-подобного фага созревание, возможно, тоже происходит при встраивании в частицу вируса или транслокации через хвост фага в клетку при инфекции», − отмечает один из авторов статьи, исследователь Центра структурной биологии и молекулярной биофизики Сили при Медицинском отделении Техасского университета Петр Лейман.
Мария Соколова подчеркивает, что это первое исследование, в котором функция crAss-подобных вирусов была рассмотрена на молекулярном и атомном уровнях. «Наша работа открывает перспективы для регулирования механизмов инфекции crAss-подобными фагами, что, в свою очередь, может стать основой для разработки новых подходов к управлению составом микробиома кишечника человека», − добавляет она.
Исследование проводилось с участием специалистов Института молекулярной генетики РАН, Института микробиологии Ваксмана при Ратгерском университете − Государственном исследовательском университете штата Нью-Джерси (США), Санкт-Петербургского политехнического университета Петра Великого, Школы остеопатической медицины при Университете Роуэн (США), Университета Линнеус (Швеция), Национального центра биотехнологической информации (США) и Медицинского отделения Техасского университета (США).
Хотя длительность помех не превышала десяти секунд, это первый известный случай такого рода. Обычно спутникам не хватает мощности для создания радиосигналов той силы, что нужна для подобных помех.
Новое исследование выявило связь между приемом глюкозамина — безрецептурной добавки от болей в суставах — и повышенным риском быстрого прогрессирования легких когнитивных нарушений в полноценную болезнь Альцгеймера.
Разработка поможет уберечь суда от экстремальных явлений погоды и обеспечит безопасную работу портов и нефтегазовых платформ в северных морях. При тестировании ИИ-модель показала отклонение менее трех процентов от эталонных данных по числу выявленных вихрей.
Хотя длительность помех не превышала десяти секунд, это первый известный случай такого рода. Обычно спутникам не хватает мощности для создания радиосигналов той силы, что нужна для подобных помех.
В 2017 году человечество впервые заметило объект, прилетевший из другой звездной системы. Он оказался странным, почти не похожим ни на астероид, ни на комету, и получил имя Оумуамуа. Затем появился «нормальный» межзвездный странник — комета Борисова. А в 2025-м астрономы обнаружили 3I/ATLAS — объект, который, вероятно, хранит вещество времен рождения чужих миров. Но что изменили в астрономии эти три гостя из межзвездной тьмы?
Астрономы провели длительную радиодиагностику межзвездного объекта 3I/ATLAS и не нашли признаков искусственных технологий. Наблюдение окончательно подтвердило естественную природу ледяного тела, хотя ученые изначально не ожидали сенсации.
В высокогорных районах Гималаев появился новый хищник. Он не боится людей, возглавляет стаи собак и все чаще заходит в деревни. Местные жители называют его «кхипшанг». Речь идет о гибриде гималайского волка и бродячей собаки. Ученые опасаются, что этот зверь изменит хрупкий баланс местной дикой природы и в скором времени станет весьма опасным для человека.
Хотя длительность помех не превышала десяти секунд, это первый известный случай такого рода. Обычно спутникам не хватает мощности для создания радиосигналов той силы, что нужна для подобных помех.
В доколумбовых Андах принадлежность к правящему роду определяла доступ к земле, торговле и статусу, поэтому удержать все внутри семьи было вопросом выживания. Ученые выяснили, что элиты долины Чинча решали эту задачу самым прямым способом — заключая браки между родственниками на протяжении как минимум двух поколений.

Вы попытались написать запрещенную фразу или вас забанили за частые нарушения.
Понятно
Что-то в вашем комментарии показалось подозрительным, поэтому перед публикацией он пройдет модерацию.
Понятно
Из-за нарушений правил сайта на ваш аккаунт были наложены ограничения. Если это ошибка, напишите нам.
Понятно
Наши фильтры обнаружили в ваших действиях признаки накрутки. Отдохните немного и вернитесь к нам позже.
Понятно
Мы скоро изучим заявку и свяжемся с Вами по указанной почте в случае положительного исхода. Спасибо за интерес к проекту.
Понятно