Нейродегенерации затрагивают все больше людей и уносят все больше жизней. Однако механизмы развития и пути лечения таких болезней, которые вызваны массированной гибелью нервных клеток, до сих пор плохо изучены. Это объясняет внимание ко все новым молекулам—участникам патогенеза нейродегенеративных болезней: болезни Альцгеймера, Паркинсона и других.
В центре внимания сотрудников ИБХ РАН и Физтех-школы биологической и медицинской физики МФТИ оказался антиген стволовых клеток простаты (prostate stem cell antigen, PSCA). Это белок, который важен при развитии рака предстательной железы и служит его биомаркером. Однако PSCA также действует на нейрональные никотиновые ацетилхолиновые рецепторы. Нарушения работы холинергической системы мозга лежит в основе многих неврологических и психических расстройств. Такая патология приводит к потери способности образовывать новые синапсы (контакты между нейронами), проблемам с вниманием, памятью и обучением. Работа опубликована в журнале Biomolecules и выполнена при поддержке гранта РНФ номер 24-14-00419.
PSCA существует в двух формах: связанной с мембраной и секретируемой. Именно вторую форму считают участвующей в развитии болезни Альцгеймера — самой распространенной нейродегенерации в мире. Заболевание встречается все чаще из-за старения населения Земли и, несмотря на огромные усилия ученых, все еще остается неизлечимым.
Исследователи полагают, что PSCA в действительности связан и со многими другими заболеваниями мозга. Дело в его способности вызывать воспалительные процессы в нервных клетках — так называемое нейровоспаление. Действительно, обнаружено, что в мозге пациентов с рассеянным склерозом, болезнью Хантингтона, при синдроме Дауна, биполярном расстройстве и слабоумии (деменции), вызванном ВИЧ-инфекцией, синтез PSCA усилен.
Чтобы детально исследовать структуру белка, а также его фармакологические свойства и роль в воспалении ученые создали искусственный (рекомбинантный) аналог PSCA — ws-PSCA. Он растворим в воде и имеет правильную конформацию, то есть трехмерную форму, которая полностью определяется последовательностью аминокислот белка и обеспечивает биологические функции молекулы.
Белок ws-PSCA всесторонне изучили, использовав целый арсенал методов биоинформатики, белковой инженерии, биофизики и нейробиологии. Ученые стремились выявить связь уровня экспрессии PSCA в мозге и развития ряда патологий нервной системы.
Белок добавляли к культуре клеток, полученных из гиппокампа. Это были как сами нейроны, так и глиальные «клетки поддержки» — астроциты. В них ws-PSCA по-разному регулировал секрецию воспалительных факторов и молекул, нужных для «слипания» клеток (клеточной адгезии).
Исследователи использовали спектроскопию гетероядерного ЯМР — метод, который позволяет визуализировать не только атомы водорода, но и некоторые другие, — а также метод релаксации азота-15 (¹⁵N). Это спектроскопическое исследование выявило трехпетельную структурную укладку молекулы ws-PSCA, состоящую из более мелких элементов структуры — зигзагообразных бета-тяжей. Однако петли II и III этой трехпетельной молекулы оказались структурно неупорядоченными. Скопление положительно заряженных аминокислот на поверхности PSCA указывает на важную роль ионных взаимодействий с участием этих двух петель белка.
Далее провели электрофизиологические эксперименты, которые помогли описать влияние ws-PSCA на состояние никотиновых ацетилхолиновых рецепторов по проходящим через мембрану токам. С этой целью использовали классическую модель — ооциты шпорцевой лягушки X. laevis. Выяснилось, что ws-PSCA ингибирует никотиновые ацетилхолиновые рецепторы типа α3β2 и как низкочувствительные, так и высокочувствительные варианты типа α4β2. При этом белок не действовал на ацетилхолиновые рецепторы α4β4. Следовательно, для его взаимодействия с рецептором необходима субъединица β2, которая в последнем случае отсутствовала.
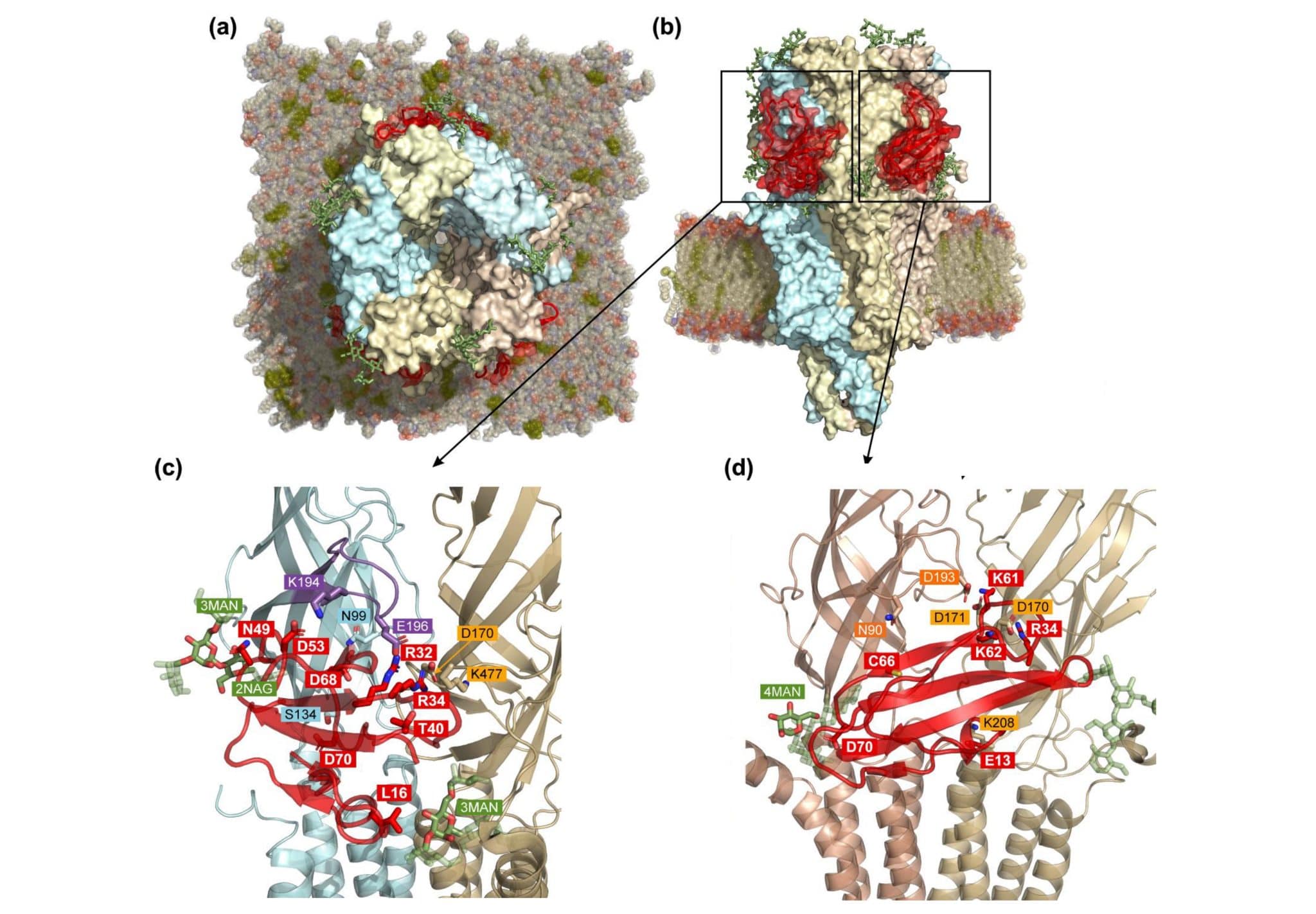
Наконец, разобраться со структурными основами взаимодействия ws-PSCA и рецепторов помогло компьютерное моделирование. А именно ансамблевый докинг и молекулярная динамика. Они показали, что ws-PSCA и его природный аналог должны распознавать интерфейс субъединиц α4/β2 и β2/β2. Образованные молекулами комплексы стабилизируют ионные и водородные связи между II и III петлями PSCA, а также главными и дополнительными субъединицами белка.
«Белки семейства Ly6/uPAR (их также называют трехпетельными из-за уникальной пространственной структуры) играют важную роль в функционировании организма человека. В нашей работе мы впервые исследовали пространственную структуру и биологическую роль трехпетельного белка PSCA. Мы показали, что, во-первых, экспрессия PSCA в мозге увеличивается и при других нейродегенеративных заболеваниях, а также при старении, и во-вторых, мишенью действия PSCA является нейрональный никотиновый рецептор α4β2 типа. Наконец, этот белок также стимулирует секрецию воспалительных факторов нейронами и астроцитами. Эта работа связывает клинические наблюдения с молекулярными механизмами и дает новый взгляд на то, как PSCA участвует в регуляции холинергической сигнализации в мозге и как это может способствовать развитию нейродегенеративных состояний», — подчеркнула Екатерина Люкманова, профессор кафедры физико-химической биологии и биотехнологии Физтех-школы биологической и медицинской физики МФТИ.