Исследователи из нескольких университетских и медицинских учреждений США в своей работе, опубликованной в издании Nature Cell Biology, сообщают о новой многообещающей стратегии преодоления лекарственной устойчивости при лейкемии и, вероятно, других злокачественных заболеваниях. Их стратегия основана на использовании целевых доз широко используемых химиотерапевтических препаратов антрациклинового ряда.
В процессе десятилетнего исследования было обнаружено, что низкие дозы антрациклинового антибиотика доксорубицина ингибируют взаимодействие между двумя молекулярными путями, которые тесно «сотрудничают», способствуя росту злокачественных процессов и устойчивости к терапии. По словам авторов исследования, еще одно неожиданное открытие — то, что целевой подход также дает возможность выполнять свои обязанности иммунным клеткам, нацеленным на пораженные раком клетки.
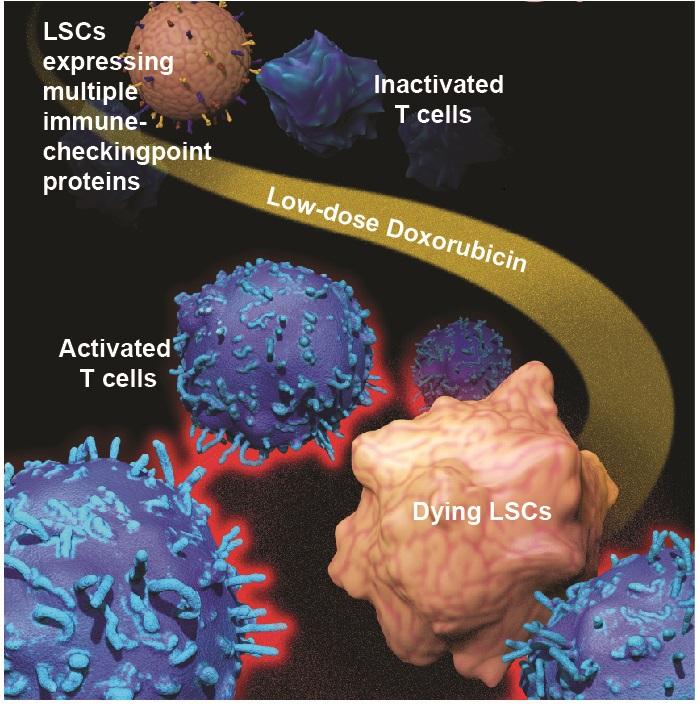
«В низких дозах доксорубицин фактически стимулировал иммунную систему, в отличие от типичных клинических доз, которые были иммуносупрессивными, убивая без разбора и здоровые иммунные клетки», — говорит первый автор работы доктор Джон М. Перри.
Вначале ученые обратили внимание на то, что протеинкиназа Akt может усиливать передачу сигналов Wnt посредством фосфорилирования бетакатенина. Это способствовало онкогенезу в кишечнике. Исследовав связанные пути Wnt/бетакатенин и PI3K/Akt в кроветворной системе на мышах с генетическими модификациями этих путей, ученые обнаружили, как они взаимодействуют. Оказалось, они стимулируют обновление стволовых клеток, что приводит к избыточной продукции кроветворных стволовых клеток. Постоянная активация путей вызывала у мышей развитие лейкемии как побочный эффект.
Подавление взаимодействия между теми же путями, дающими «зеленый свет» стволовым клеткам, на базе которых размножаются клональные клетки лейкемии, позволило бы справиться с болезнью. Однако многие лекарства, которые непосредственно нацелены на пути Wnt/бетакатенин или PI3K/Akt, в итоге терпят неудачу, потому что раковые клетки развивают устойчивость к ним, а химиотерапевтические препараты широкого действия могут иметь резкие побочные эффекты и системную токсичность.
Целью ученых был поиск такого препарата, который сможет блокировать взаимодействие между Wnt/бетакатенином и PI3K/Akt и при этом не быть чрезмерно токсичным. Для этого они рассмотрели библиотеку уже существующих препаратов, чтобы определить, как их можно направить на несколько измененную задачу.
Скрининг показал, что доксорубицин наилучшим образом подавляет взаимодействие между двумя путями. Его ингибирующие свойства при низких дозах имеют преимущество по сравнению с высокодозовым применением в качестве химиотерапевтического препарата, при котором он может вызвать серьезное повреждение сердца.
Тестирование провели на мышах, которым подсаживали образцы резистентных и нерезистентных клеток, взятые у больных лейкемией детей. «Мы обнаружили, что у мышей, которым трансплантируют образцы пациентов с резистентными к терапии стволовыми клетками лейкоза, быстро развивается лейкоз, но лечение доксорубицином в низких дозах улучшает выживаемость за счет сокращения стволовых клеток лейкемии, — говорит доктор Перри. — При этом мыши, получавшие трансплантаты образцов пациентов, которые не содержали резистентных к терапии стволовых клеток лейкемии, не реагировали на лечение низкими дозами доксорубицина. Эти результаты показали, что хеморезистентные стволовые клетки лейкемии у пациентов могут быть функционально снижены при лечении низкими дозами доксорубицина, по крайней мере, в тестах на модельных животных».
В последующем клиническом тестировании на взрослых людях, устойчивых к лечению острого миелобластного лейкоза, половине больных помог низкодозовый даунорубицин (химиопрепарат того же класса, что и доксорубицин). У них был ответ на лечение и уменьшение количества стволовых клеток лейкемии, имеющих активированный Akt биомаркер бетакатенина.
Кроме прочего, ученым удалось узнать больше о механизме, который обеспечивает раковым клеткам возможность уклоняться от иммунного ответа. Они обнаружили, что стволовые клетки лейкемии экспрессируют множество белков, известных как иммунные контрольные точки, отключающие иммунный ответ, который в противном случае распознал и устранил бы стволовые клетки лейкемии. Кроме того, бетакатенин связывается с несколькими локусами гена иммунной контрольной точки. Обработка низкими дозами доксорубицина снижала экспрессию этих иммунных контрольных точек, включая PD-L1, TIM3 и CD24.
Дальнейшие исследования команды направлены на тестирование аналогичных стратегий для преодоления устойчивости к терапии таких видов рака, как рак молочной железы, толстой кишки и глиобластома.
Данные работы позволят создать более эффективную стратегию для преодоления резистентности к терапии рака и стимулирования иммунитета, которую можно использовать в сочетании с другими видами лечения рака, включая химио-, иммуно- и лучевую терапию для пациентов с лейкемией и другими видами рака. Низкие дозы, кроме прочего, позволяют избежать резких побочных эффектов высоких доз доксорубицина и родственных препаратов, потенциально предлагая пациентам лучшее качество жизни.