Условно-патогенные бактерии — клебсиеллы — относятся к семейству Enterobacteriaceae и считаются представителями нормальной микрофлоры кишечника здоровых людей. Эти прямые грамотрицательные палочки, образующие капсулы, как правило, неподвижны и растут на простых питательных средах.
Некоторые виды клебсиелл, однако, служат наиболее частыми возбудителями пневмонии, кишечных и урогенитальных инфекций у пациентов с ослабленным иммунитетом. В 2017 году эксперты Всемирной организации здравоохранения причислили клебсиеллы к наиболее опасным бактериальным патогенам в связи с их растущей устойчивостью к антибактериальным препаратам.
Недавно исследовательская группа под руководством Тревора Литгоу (Trevor Lithgow) собрала образцы из водных резервуаров Вурунтьери и обнаружила в них два подтипа бактериофага Merri-merri-uth nyilam marra-natj (MMNM), который инфицирует бактерию Klebsiella pneumoniae.
Хотя оба подтипа оказались практически идентичны, один из них, обозначенный как MMNM (Ala134), показал сниженную активность против полирезистентного штамма клебсиеллы AJ174-2 (полирезистентными называют бактерии, которые обрели устойчивость к двум и более антибиотикам).
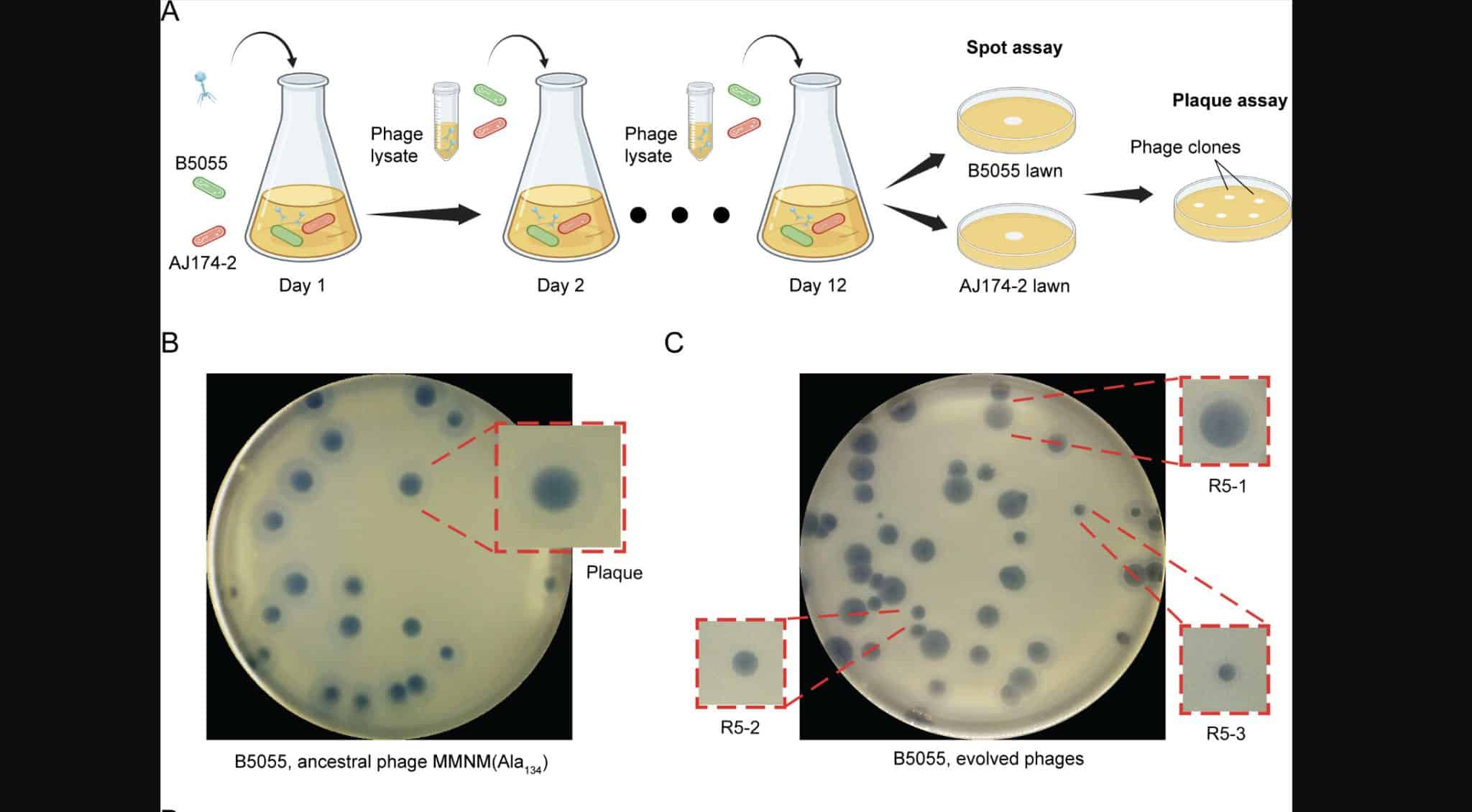
Именно это небольшое отличие легло в основу дальнейших экспериментов по изучению эволюции фагов. В частности, ученые провели серию экспериментов, подвергнув фаг MMNM (Ala134) воздействию полирезистентного штамма клебсиеллы AJ174-2, вызывающего пневмонию.
В результате исследователи получили 20 новых вариантов фага с различными фенотипическими проявлениями.
Дальнейшее секвенирование генома новых вариантов помогло выявить мутации в небольшом наборе белков, составляющих базальную пластинку вируса, которые играют ключевую роль в процессе инфицирования бактерий. Так как именно от базальной пластинки отходят тонкие длинные нити, помогающие фагам прикрепляться к бактериям, даже небольшие изменения в ее структуре могут повлиять на эффективность заражения.
Напомним, в отличие от антибактериальных препаратов, уничтожающих как болезнетворные патогены, так и представителей нормальной микрофлоры, фаги более избирательны и атакуют микроорганизмы определенного вида, поддерживая микрофлору в борьбе с инфекцией. Ранее считалось, что фаги эволюционируют преимущественно путем крупной генетической перестройки, например с помощью рекомбинации генов, которая приводит к мозаицизму — наличию генетически различающихся клеток.
Однако результаты нового исследования, опубликованного в журнале mBio, показали, что даже небольшие точечные мутации могут привести к эволюционным изменениям, позволяя бактериофагам быстро адаптироваться к новым хозяевам и условиям окружающей среды.
«Все разработанные нами фаги могут убивать клебсиеллу, но некоторые разновидности делают это лучше, чем другие», — отметили авторы научной работы.
Понимание эволюционных и адаптационных механизмов фагов имеет важное значение для разработки новых методов борьбы с инфекциями, устойчивыми к современным антибиотикам. Открытие дарит надежду на существование пока неизвестных природных популяций фагов, обладающих генетическими вариациями и способных уничтожать супербактерии. Работа также расширяет понимание микроэволюционных процессов и имеет важное значение для изучения генетического разнообразия вирусных популяций.