Результаты исследования опубликованы в журнале Communications Biology. Работа выполнена при поддержке Министерства науки и высшего образования Российской Федерации и Российского научного фонда. Клетки человека постоянно реагируют на получаемую от соседних клеток и от окружающей среды информацию. За большую часть реакций на окружение отвечают семиспиральные белки, также называемые GPCR (G-protein-coupled receptors, или рецепторы, сопряженные с G-белком).
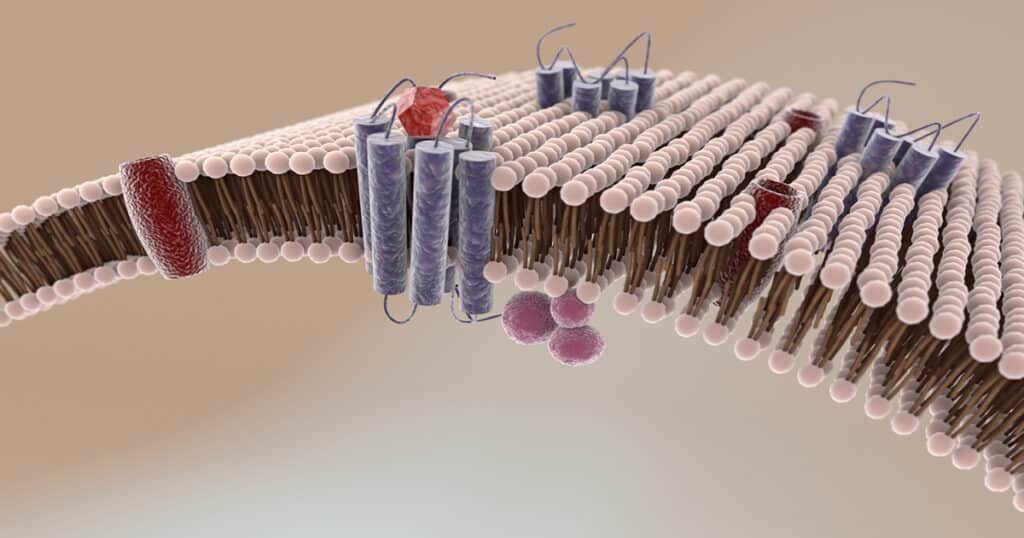
Они состоят из семи пронизывающих клеточную мембрану спиралей, один конец которых обращен внутрь клетки, а другой — наружу. Изменение поведения белковых спиралей и вызывает клеточный ответ. Нарушения работы рецепторов могут приводить ко множеству болезней, в том числе аллергии, астме и некоторым психическим заболеваниям. Поэтому такие белки стали мишенями для более чем трети одобренных к использованию лекарств.
GPCR — это сложные молекулярные «переключатели», которые, как правило, имеют не только состояния «on» и «off». Они крайне подвижны и имеют несколько относительно стабильных состояний — конформаций, приводящих к различным клеточным ответам. Переключение GPCR из одного состояния в другое называют конформационной динамикой. Зная, как часто белок принимает определенную форму и насколько долго в ней находится, ученые могут с большей точностью и скоростью подбирать молекулы, которые вызывают необходимый клеточный ответ.
Один из наиболее удобных для исследования GPCR — аденозиновый рецептор, который среди прочего является главной молекулярной мишенью для кофеина. В научной литературе уже собрано много данных о его структуре и функциях, с которыми можно сравнить свои результаты. Биофизики из Центра исследований молекулярных механизмов старения и возрастных заболеваний МФТИ изучили конформационную динамику аденозинового рецептора с помощью метода FRET (Förster Resonance Energy Transfer, фёрстеровский резонансный перенос энергии).
При таком исследовании находящиеся рядом части рецептора помечаются двумя флуоресцирующими метками, синей и красной, яркость свечения которых сильно зависит от расстояния между ними. При изменении состояния GPCR расстояние между метками изменяется, а вместе с ним и цвет, который создают метки: в более «синих» молекулах метки дальше друг от друга, а в более «красных» — ближе между собой. Наблюдая за изменениями цвета одиночных молекул с помощью сверхчувствительного оптического микроскопа, биофизики проследили переключение белка между несколькими состояниями и измерили времена нахождения белка в них. Данный подход позволил определить, как на конформационную динамику GPCR влияет взаимодействие с активирующими химическими соединениями.
«В этой работе мы не только исследовали динамику аденозинового рецептора, но и продемонстрировали, что метод ее изучения можно применять к GPCR. Ранее не удавалось исследовать семиспиральные белки методом FRET на уровне одиночных меолкул. Данный подход позволяет исследовать белок в условиях, максимально близких к природным, и получать крайне важные данные для понимания взаимодействия белка с активными веществами. Благодаря знаниям о состояниях GPCR можно быстро разрабатывать и тестировать новые лекарства от болезней, вызываемых нарушением работы белков. В частности, рецептор, который мы исследовали в работе, является многообещающей мишенью для лекарств от бессонницы, депрессии и болезни Паркинсона», — рассказывает Валентин Борщевский, заместитель директора Центра исследований молекулярных механизмов старения и возрастных заболеваний МФТИ.
Авторы построили полную биофизическую модель активации белка, отражающую его функциональную конформационную динамику. Это никогда раньше не делалось на уровне одной молекулы для данного рецептора или другого GPCR.