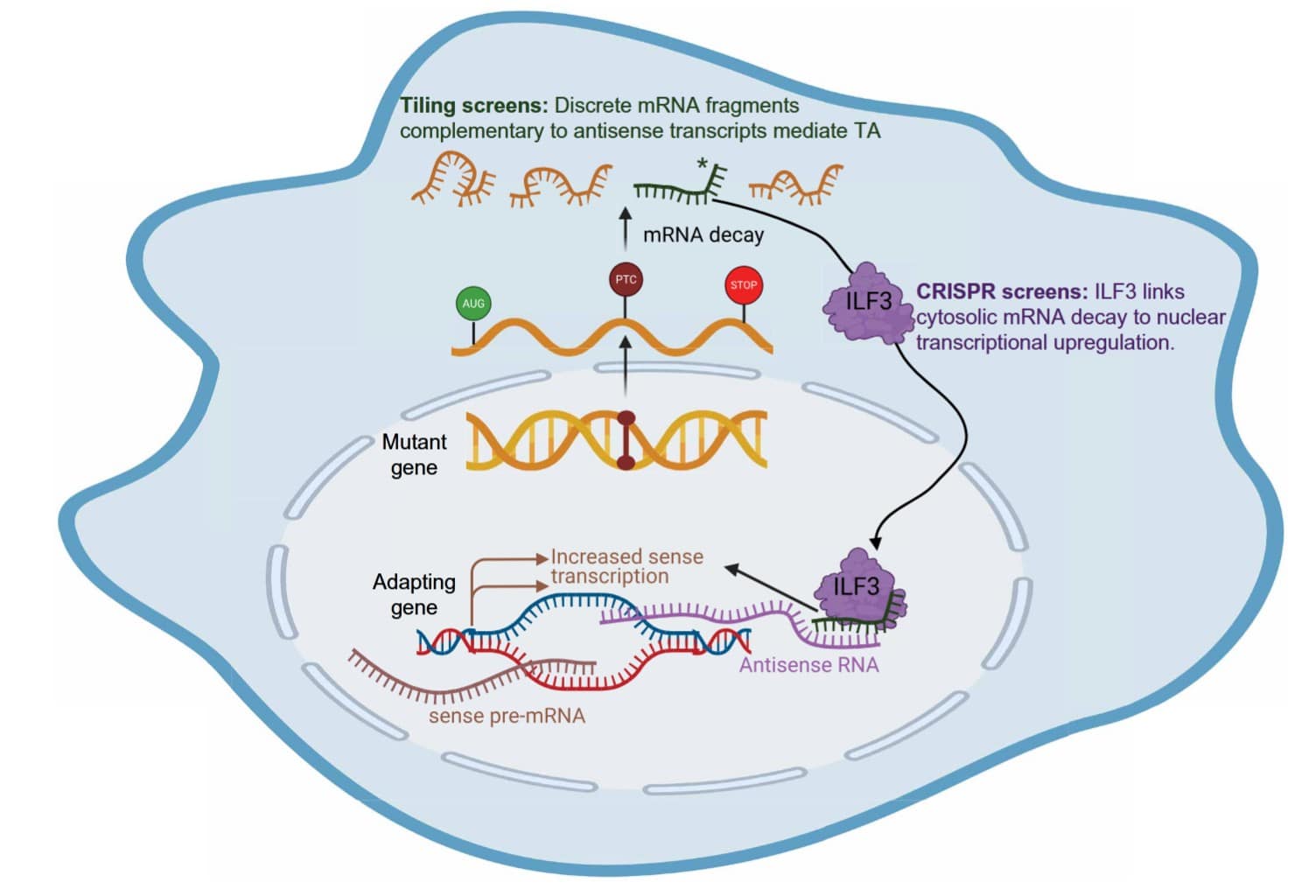
В клетках существуют механизмы, которые исправляют или компенсируют поломки в генах. Один из защитных механизмов называется «транскрипционная адаптация». Работает он так: обнаружив дефектную матричную РНК (мРНК), клетка уничтожает ее, но использует продукты распада как сигнал бедствия. Этот сигнал заставляет активироваться здоровые гены-дублеры (паралоги), которые берут на себя функции сломанного.
Долгое время оставалось загадкой, как именно информация о поломке передается из цитоплазмы, где утилизируется мусор, в ядро, где хранится ДНК и происходит синтез новых молекул.
Авторы исследования, опубликованного в журнале Science, использовали модельные клетки мышей с мутацией в гене актина (Actg1), в норме вызывающей компенсаторную активность другого гена (Actg2). С помощью полногеномного CRISPR-скрининга ученые поочередно выключали тысячи генов, чтобы найти тот, без которого механизм защиты перестает работать.
Дополнительно в клетки вводили тысячи синтетических фрагментов РНК разной длины, чтобы выяснить, какая именно последовательность служит кодом активации для спасательного механизма. Биохимическими методами ученые отследили, с какими участками генома взаимодействует белок-посредник.
Анализ помог выявить белок ILF3 как главное звено процесса. Он захватывает фрагменты уничтоженной мутантной РНК в цитоплазме и переносит их в клеточное ядро. Там этот комплекс находит комплементарную фрагменту РНК антисмысловую цепочку на ДНК здорового гена-паралога.
Связавшись с целью, ILF3 меняет структуру хроматина, делая его более доступным, и ускоряет процесс считывания генетической информации (элонгацию).
Ученые доказали, что систему можно использовать в терапевтических целях. Введение в клетку короткого синтетического кусочка РНК (имитирующего обломок) заставило ее включить здоровый ген PKD1, дефект которого вызывает поликистоз почек. При этом само наличие реальной поломки в геноме оказалось необязательным — достаточно было ввести ложный сигнал об аварии.
Открытие предлагает стратегию лечения генетических заболеваний без вмешательства в саму ДНК. Вместо сложной починки мутаций методами генной инженерии врачи смогут использовать короткие олигонуклеотиды, чтобы принудительно активировать спящие здоровые копии или функциональные аналоги сломанных генов.